糖尿病是一種全球流行性疾病,美國糖尿病學會(ADA)年會是一年一度內分泌領域糖尿病相關的學術盛會。第 83 屆 ADA 年已會於 2023 年 6 月 23 日拉開帷幕,共 4 天議程。
糖尿病周圍神經病變(DPN)是糖尿病最常見的並發癥之一,嚴重影響糖尿病患者的生活質量。本屆 ADA 年會特設「糖尿病周圍神經病變有關的新興技術和治療方法」專題,讓我們一起來瞭解一下 ADA 年會上研究者們的新發現。
新進展一
功能磁共振 + 機器學習探索 PDPN 亞型
「知己知彼,百戰不殆」,對疾病的有效治療往往需要對疾病的發病機制、臨床特征有深入瞭解。
本屆 ADA 年會上,英國謝菲爾德大學的 Dinesh Selvarajah 博士(圖 1)介紹瞭利用靜息態功能磁共振成像(RS-fMRI)技術對痛性糖尿病周圍神經病變(PDPN)患者進行腦部掃描,再聯合無監督機器學習方法可獲得 PDPN 不同的 RS-fMRI 功能連接亞型,從而對治療結果進行預測。

圖 1(圖片來自 ADA 網站)
Dinesh Selvarajah 博士團隊的研究納入瞭 82 例 PDPN 患者和 36 例健康志願者進行 RS-fMRI 掃描。PDPN 受試者被分為訓練集(n = 48)和測試集(n = 34)。通過無監督機器學習(k-Means 算法)分析關鍵體感/傷害性腦區的 RS-fMRI 功能連接性,以識別臨床疼痛亞型。
結果顯示,RS-fMRI 功能連接可定義兩種臨床相關的 PDPN 亞型,兩種亞型在後中央(p < 0 xss=removed>
此外,同側區域的腦功能連接、腦默認網絡的 RS-fMRI 功能連接也存在顯著差異。無監督機器學習模型可以預測治療反應性,準確度為 0.77,召回率為 0.83,精確度為 0.83,曲線下面積(AUC)為 0.73(圖 2)。
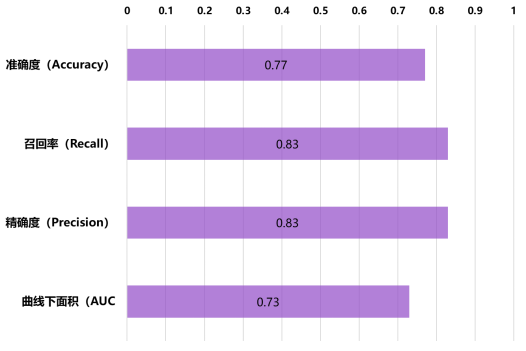
圖 2(根據數據制作)
該研究的發現顯示腦功能連接與健康對照組差異越大的亞型,其對 PDPN 的治療反應越差。
該研究提示,RS-fMRI + 機器學習的模式對 PDPN 的治療結果的預測有較高的精度,這可能是一種潛在有效的臨床分類方式,但仍需在更大樣本中進行驗證。
新進展二
新型非阿片類止痛藥
對 PDNP 進行有效的口服藥物治療歷來備受關註和挑戰。LX9211 是銜接子相關蛋白激酶-1(AAK1)抑制劑,該藥物是一種非阿片類、且作用於新靶點的止痛藥。
本屆 ADA 年會,來自密歇根大學的 Rodica Busui 博士(圖 3)展示瞭 LX9211 隨機、雙盲、安慰劑對照、平行組、多中心的 2 期臨床試驗(RELIEF-DPN 1 研究)結果。

圖 3 (圖片來自 ADA 網站)
研究納入 319 名 PDNP 成年患者,平均年齡為 62.2 ± 9.94 歲,平均糖化血紅蛋白 A1c 值為 7.7% ± 1.28%,平均 BMI 為 32.07 ± 4.45 kg/m2,安慰劑預處理後平均每日疼痛評分(ADPS)為 6.55 ± 1.089。
患者被隨機分配到安慰劑組、LX9211 低劑量組(第 1 天使用 100 mg,之後使用 10 mg)、或 LX9211 高劑量組(第 1 天使用 200 mg,之後使用 20 mg)治療 6 周。之後進行 5 周安全期隨訪。
有效性方面,治療第 6 周,LX9211 幹預組實現瞭主要終點(ADPS 變化量)的改善。與安慰劑相比,LX9211 低劑量組神經病理性疼痛癥狀評價量表(NPSI)總分降低瞭 5.18 分(p = 0.064)、高劑量組 NPSI 總分降低瞭 7.22 分(p = 0.008),且 LX9211 低劑量組和高劑量組均顯著改善瞭患者燒灼痛癥狀及疼痛對睡眠的幹擾情況。
此外,與安慰劑相比,LX9211 低劑量組還顯著降低瞭患者整體印象變化量表評分(p = 0.031)。安全性方面,LX9211 使用者未發生治療相關的嚴重不良事件或死亡,並且 LX9211 的使用不會影響受試者重要心血管代謝指標(包括體重、血壓、血糖、膽固醇)水平。
RELIEF-DPN 1 試驗表明 LX9211 是一類具有治療前景的、可改善 PDNP 癥狀的非阿片類藥物。關於 LX9211 的安全性和有效性計劃在未來的 3 期臨床試驗中繼續進行認證。
新進展三
魚油中的 ω-3 多不飽和脂肪酸(PUFA)
既往研究顯示來自魚油的 ω-3 PUFA 對糖尿病血管和神經病變有一定治療效果。在本屆 ADA 年會上,來自愛荷華大學的 Mark A Yorek 博士(圖 4)特別關註瞭 ω-3 PUFA 的不同來源是否影響 DPN 的治療效果。

圖 4(圖片來自 ADA 網站)
研究采用瞭 2 型糖尿病大鼠模型。在大鼠進行 10 周高血糖建模後,給予各種不同來源的 ω-3 PUFA 補充劑治療 12 周,包括魚油、磷蝦油、藻類油(主要提供 EPA 或 DHA,或同時提供 EPA 和 DHA)或商業化制劑(含 EPA、DHA 或 EPA 和 DHA)。
研究的主要終點包括運動神經傳導速度和感覺神經傳導速度、表皮內和角膜內神經纖維密度、熱敏感性和角膜敏感性,以及為坐骨神經提供循環的神經外膜小動脈的血管反應性。同時研究者對 ω-3 指數和血清脂肪酸水平也進行瞭測定。
每種 ω-3 PUFA 補充劑的劑量都是定制的,以達到一個健康的 ω-3 指數(其定義為 EPA 和 DHA 的總和占紅細胞中總脂肪酸的百分比,范圍為健康水平的 8 ~ 12%)。
研究結果顯示,與對照組相比,未經治療的糖尿病大鼠的神經和血管終點指標明顯受損。采用魚油治療後所有神經相關的終點效應改善效果最大,其次是磷蝦油、藻類油(同時提供 EPA 和 DHA)或商業化制劑(含 EPA 和 DHA)。
單一 ω-3 PUFA 來源的藻類油(提供 EPA 或 DHA)或商業化制劑(含 EPA 或 DHA)的改善效果最差。
此外,使用魚油治療後,神經外膜小動脈對乙酰膽堿的血管反應性得到瞭最大改善,而其他來源的 ω-3 PUFA 補充劑對其改善效果較小。
基於上述動物模型的臨床前研究證據表明,在治療 DNP 的臨床試驗中,使用魚油作為 ω-3 PUFA 的來源可能會獲得最好的治療效果。
新進展四
德谷樣胰島素類似物
既往降糖藥物無法有效治療 DPN。來自丹麥的 Thorbjörn CA Åkerström 博士分享的內容是探索一種新型胰島素 —— 德谷樣胰島素類似物是否在降血糖的同時還能改善 DPN。
該研究中,德谷樣胰島素類似物 B 鏈上不存在末端蘇氨酸,但與德谷胰島素具有相同的藥代動力學和藥效動力學。研究采用糖尿病大鼠模型,使用德谷樣胰島素類似物或者對照基礎胰島素(IC)治療 18 周,另外還包括一組健康對照大鼠模型。
研究觀察指標包括感覺神經和運動神經傳導速度、痛覺過敏實驗、熱敏感性、角膜敏感性、感覺神經的神經支配以及神經外膜小動脈的血管反應性。
研究結果顯示,德谷樣胰島素類似物與 IC 有相當的降糖效果,並且改善瞭神經病變相關的指標參數。治療結束時,幹預組大鼠的熱敏感性、角膜敏感性、角膜神經纖維長度、感覺和運動傳導速度與健康對照組大鼠相比無統計學差異。這提示相較於 IC,德谷樣胰島素類似物對 DPN 的改善效果更明顯。
該臨床前研究表明德谷樣胰島素類似物在控制血糖的同時能夠有效改善 DNP,或許可以同時發揮既控制血糖又治療 DPN 的「一箭雙雕」的作用。
除嚴格控制血糖外,藥物是治療 DPN(包括 PDPN)的重要手段,但目前已有的治療 DPN 的藥物普遍療效有限。上述研究顯示出瞭令人期待的初步成果,對進一步的研究有哪些啟示、離臨床應用又有多遠呢?
丁香園內分泌時間邀請到四川大學華西醫院童南偉教授、張舫副教授,進行點評與解答。
點評專傢


點評內容
DPN 最主要的是一種感覺神經異常,可累及自主神經系統,且通常隨著疾病進展會出現運動神經的異常。任何年齡均可發病,且男女發病率無明顯差異。目前 DPN 確切的發病機制尚不明瞭,研究顯示與神經缺血缺氧、氧化應激、神經營養因子缺乏、多元醇通路活性異常增加等機制有關。
DPN 的危險因素目前已在多項大型橫斷面和前瞻性研究中得到證實,包括血糖控制欠佳、年齡和病程的增長、肥胖、腰臀比增加、高血壓、血脂異常、高甘油三酯血癥、吸煙以及遺傳多態性差異等。因此,DPN 的管理強調綜合性和個體化。
盡管目前已有治療 DPN 的不同上市藥物,但普遍療效有限。所以,針對 DPN 的不同亞型的早期識別和基於機制改善病情的藥物開發,是現今相關領域的研究熱點。
本屆 ADA 對 DPN 的展望既涉及運用 RS-fMRI + 機器學習的方法對患者進行中樞神經系統成像以預測 PDPN 治療效果的前瞻性預測分層,又涵蓋瞭非阿片類新型止痛藥 LX9211 的 2 期臨床試驗結果匯報,還包括多項在動物模型中進行的臨床前研究。
總體而言,上述研究都顯示出令人期待的初步成果。但值得註意的是,之前也有一些 DPN 治療藥物雖然在糖尿病嚙齒類動物模型或者 2 期臨床研究中展示出積極的發現,但在後續研究中卻並沒有得到令人滿意的結果。
故而,上述研究報道的相關發現還需要在之後的大樣本或後續臨床試驗中進行探索和證實。
綜上所述,盡管本屆 ADA 中 DPN 的多項研究結論尚待進一步認證,但研究者們從涉獵 AI 的疾病臨床分型、新型止痛藥物的開發到不同來源 ω-3 PUFA 的效果區分、德谷樣胰島素類似物一藥多效的初步探索,都為 DPN(包括 PDPN)的臨床診治前景帶來瞭新的曙光。
期待未來 DPN 不僅有藥可用、多藥可選,而且藥物治療效果可提前預判,根據發病機制選擇對應藥物、甚至實現一藥多效的治療效果。
策劃 | 戴冬君



發表評論 取消回复