在中樞神經系統腫瘤中,神經膠質瘤占大多數。根據世界衛生組織(WHO)的分級,1 級和 2 級膠質瘤生長較為緩慢,被稱為 「 低級別膠質瘤 」;而 3、4 級膠質瘤的進展較為迅速,被稱為 「 高級別膠質瘤 」[1]。
在低級別彌漫性膠質瘤中,IDH1/2 突變較為常見,且這部分患者的預後相比 IDH 野生型明顯更佳。然而,新診斷的 IDH1/2 突變膠質瘤尚無可以治愈的治療方案。患者經過最大程度的安全切除手術後,進行放化療,或者經過觀察檢測後必要時進行放化療。
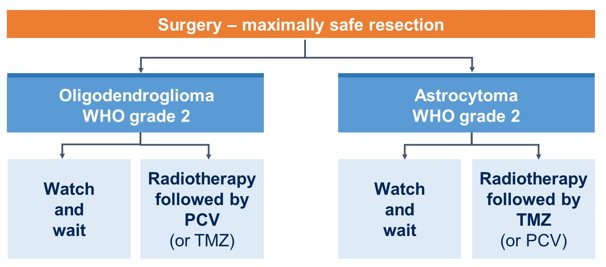
新診斷 IDH1/2 突變膠質瘤的診療路徑 [2]
然而,手術和術後放化療無法治愈低級別膠質瘤,並可能導致長期毒副反應。Vorasidenib 是一種口服 IDH1/2 雙重抑制劑,可透過血腦屏障。本次 2023 美國臨床腫瘤學會(ASCO)年會全體大會上公佈瞭 INDIGO III 期臨床研究的重磅結果(摘要號:LBA1),該研究同步發表在 NEJM [3]。這是 23 年來低級別膠質瘤治療方面的首次重大進展,也意味著 IDH1/2 突變的低級別膠質瘤正式有瞭靶向治療藥物。

NEJM 截圖
23 年來首次重大突破,INDIGO 研究改寫低級別膠質瘤治療格局
INDIGO 研究是一項 III 期全球、雙盲、隨機對照臨床研究,探索 Vorasidenib(口服 IDH1/IDH2 抑制劑)vs 安慰劑治療 IDH1/IDH2 突變 2 級彌漫性膠質瘤的療效和安全性。
研究納入 ≥12 歲、不需要立即化療或放療的 IDH1/2 突變的 2 級少突神經膠質瘤和星形膠質細胞瘤(根據 2016 年 WHO 指南),集中確認 IDH1/2 狀態,既往僅接受手術,可評估的無強化疾病(≥1 個靶病灶 ≥1 cm×≥1 cm)。患者按 1:1 的比例隨機分至 Vorasidenib 組和安慰劑組,經過集中評估疾病進展的安慰劑組患者可以揭盲並交叉至 Vorasidenib 組治療。研究主要終點為盲態獨立評審委員會(BICR)評估的無進展生存期(PFS),次要關鍵終點為至下次幹預的時間(TTNI)。
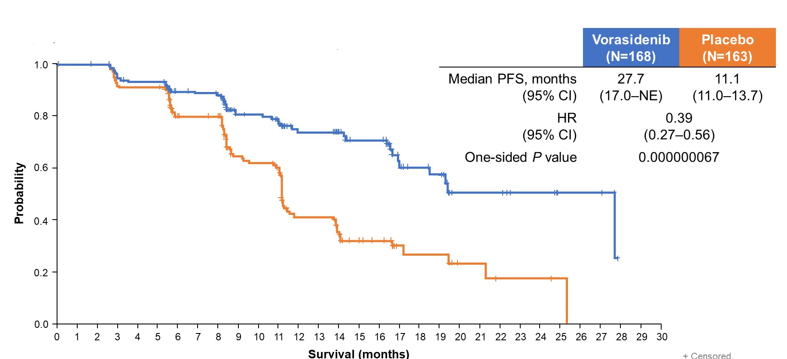
截至 2022 年 9 月,共有 10 個國傢 77 個中心參與試驗。研究共納入 331 名患者,中位年齡為 40.4 歲(范圍,16-71 歲)。結果顯示,226 位患者仍在接受治療;Vorasidenib 組的中位 PFS 為 27.7 個月(95%CI 17.0 個月-NE),而安慰劑組的中位 PFS 為 11.1 個月(95%CI 11.0-13.7 個月),HR = 0.39(95%CI 0.27-0.56)。差異具有統計學意義。
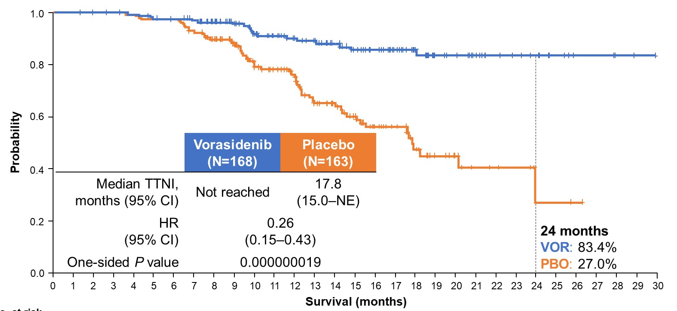
Vorasidenib 組的中位 TTNI 未達到,安慰劑組的 TTNI 為 17.8 個月(95%CI 15.0-NE),HR = 0.26(95%CI 0.15-0.43)。值得註意的是,到 24 個月時,Vorasidenib 組不接受其他療法的患者比例為 83.4%,而安慰劑組為 27.0%。
在安全性方面,Vorasidenib 組發生 ≥3 級治療期間不良事件(TEAEs)發生率為 22.8%(安慰劑組為 13.5%),因 TEAE 導致的治療中斷發生率為 29.9%(安慰劑組 22.7%),因 TEAE 導致的減量發生率為 10.8%(安慰劑組 3.1%),因 TEAE 導致的停藥發生率為 3.6%(安慰劑組 1.2%)。
Vorasidenib 組對比安慰劑組的 AE 分別是谷丙轉氨酶升高(38.9% vs 14.7%)、新冠病毒感染(32.9% vs 28.8%)、疲勞(32.3% vs 31.9%)、天冬氨酸轉氨酶升高(28.7% vs 8.0%)、頭痛(26.9% vs 27.0%)、腹瀉(24.6% vs 16.6%)、惡心(21.6% vs 22.7%)。常見 3 級 AE(>5%)為谷丙轉氨酶升高(9.6% vs 0%)。
該研究證實,對於無需立即放化療的 IDH1/2 突變 2 級膠質瘤患者,Vorasidenib 可有效延長其 PFS 和 TTNI,延緩接受放化療的時間。
INDIGO 研究引領低級別膠質瘤進入靶向治療時代
INDIGO 研究是首個探索 2 級膠質瘤靶向治療的臨床試驗,將低級別膠質瘤帶入靶向治療時代。目前,Vorasidenib 在全球范圍內尚未獲批上市,期待其盡快給低級別膠質瘤患者帶來靶向治療選擇。
此外,今年 2 月,Nature Medicine 發表瞭一項 Vorasidenib 對比另一種 IDH1 抑制劑艾伏尼佈治療 IDH1 突變低級別膠質瘤的 1 期研究。在抗腫瘤活性、治療持續時間上,兩個藥顯示出相似的水平。安全性方面,兩種藥物耐受性良好,未發生治療相關的治療延遲 [4]。2020年JCO公佈瞭艾伏尼佈治療IDH1突變晚期膠質瘤的研究數據,在66例mIDH1晚期膠質瘤患者中,艾伏尼佈耐受性良好,未見劑量限制毒性報道,未達到最大耐受劑量 [5]。
隨著越來越多的IDH抑制劑湧現並取得瞭令人期待的積極研究結果,IDH 突變膠質瘤即將迎來全新的靶向時代。
延緩放化療時間,為患者帶來更好生命體驗
在全體大會上,Rimas V. Lukas 教授對 INDIGO 研究的意義以及未來膠質瘤的治療發表瞭看法。
目前,臨床對於低危的 2 級膠質瘤予以術後觀察處理,對於高危的 2 級膠質瘤予以放療+化療。RTOG 9802 研究顯示,對於高危 IDH1 突變的 2 級膠質瘤患者,放化療可帶來 PFS、OS 獲益 [6]。對於 IDH1/2 突變 2 級膠質瘤患者,目前整體生存預後較好,12 個月的 OS 率為 98% [7]。
但是,放療對正常腦組織的功能存在影響,對患者生存質量影響較大。因此,推遲放療,延緩認知功能衰退對患者意義重大。INDIGO 研究證實,IDH 抑制劑為這部分患者提供療效更好、損傷更小、生活質量更高的治療方案。
未來,對於 IDH 抑制劑耐藥機制、其他有效的分子亞型以及聯合治療方案均是未來發展方向。
參考文獻:
[1] Louis DN, Perry A, et al. The 2021 WHO Classification of Tumors of the Central Nervous System: a summary. Neuro Oncol. 2021;23(8):1231.
[2] Figure modified from:Weller M et al. Nat Rev Clin Oncol 2021;18:170-86.
[3] Mellinghoff IK, van den Bent MJ, Blumenthal DT, et al. Vorasidenib in IDH1- or IDH2-Mutant Low-Grade Glioma. N Engl J Med. 2023;10.1056/NEJMoa2304194. doi:10.1056/NEJMoa2304194.
[4] Mellinghoff IK, et al. Vorasidenib and ivosidenib in IDH1-mutant low-grade glioma: a randomized, perioperative phase 1 trial. Nat Med. 2023 Mar;29(3):615-622.
[5] Mellinghoff IK, et al. Ivosidenib in Isocitrate Dehydrogenase 1-Mutated Advanced Glioma. J Clin Oncol. 2020 Oct 10;38(29):3398-3406.
[6] Buckner JC, et al. NEJM. 2016;374(14):1344-1355.
[7] Ostrom QT, et al. Neuro Oncol. 2023;25(4):799-807.
作者:sweet;編輯:Huan
排版:樂樂





發表評論 取消回复