在我國,胃癌的發病率、死亡率均位居惡性腫瘤的第三。2020 年,中國約有 37 萬人因胃癌死亡 [1]。然而,胃癌是一種高度異質性的惡性腫瘤,傳統療法對胃癌治療效果不佳,精準治療或許可以成為改善晚期胃癌患者生存預後的破局之法。
靶向治療是胃癌綜合治療格局的重要組成部分。近年來,胃癌靶向治療的臨床研究眾多,但目前的進入臨床的僅有 HER2 藥物曲妥珠單抗和抗血管生成藥物阿帕替尼,期待更多新療法給胃癌患者帶來新的希望。Claudin 18.2 作為一種在胃癌細胞中高表達的治療靶點,屢屢在各大學術會議上被提及。Claudin 18.2 的靶向治療藥物研究進展如何?還有多久可以進入臨床,造福患者?
2023 年美國臨床腫瘤學會(ASCO)年會在美國芝加哥召開。中山大學腫瘤防治中心的徐瑞華教授在會上進行以 「III 期 Glow 研究主要結果更新:Zolbetuximab 聯合 Capox 一線治療 Claudin 18.2 高表達/HER 陰性的局部晚期或轉移性胃/胃食管結合部腺癌 Updates on Abstract 405736: Zolbetuximab + Capox in 1L Claudin-18.2+ (CLDN18.2+)/HER2− Locally Advanced (LA) or Metastatic Gastric or Gastroesophageal Junction (mG/GEJ) Adenocarcinoma: Primary Phase 3 Results from Glow.」 為題的報告。丁香園腫瘤時間「2023 ASCO 中國之聲」欄目邀請徐瑞華教授就該研究的主要結果進行解讀。

徐瑞華教授在 ASCO 口頭匯報現場
GLOW 研究 III 期結果發佈,
或成晚期胃癌新標準方案
GLOW 是全球多中心臨床研究,共 18 個國傢、地區,166 傢醫院參加。該研究探索瞭 Zolbetuximab + CAPOX 一線治療在 CLDN18.2+/HER2-局部晚期或轉移性胃或胃食管交界處腺癌患者中的療效和安全性 [2]。
研究納入初治 Claudin 18.2 陽性/HER2 陰性局部晚期不可切除或轉移性胃/胃食管結合部腺癌患者,ECOG OS 0-1。按照 1:1 的比例隨機分配至 Zolbetuximab+CAPOX 組(254 例)或安慰劑+CAPOX 組(253 例),經 8 周期治療後,患者繼續使用 Zolbetuximab+卡培他濱或安慰劑+卡培他濱治療。主要研究終點為基於RECIST v1.1無進展生存期(PFS),關鍵次要終點為總生存期(OS),其他次要終點包括客觀緩解率(ORR)、緩解持續時間(DoR)和安全性等。
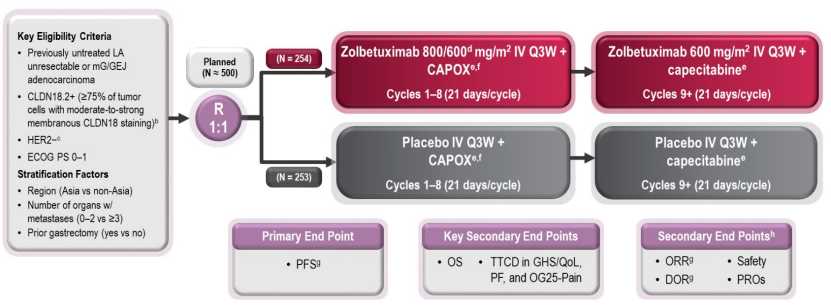
圖 1. GLOW 研究設計
結果發現,Zolbetuximab 聯合 CAPOX 組對比安慰劑+CAPOX 組的 mPFS 為 8.21 個月 vs 6.80 個月,Zolbetuximab 聯合 CAPOX 降低疾病進展或死亡風險 31.3%(HR = 0.687;P = 0.0007)。
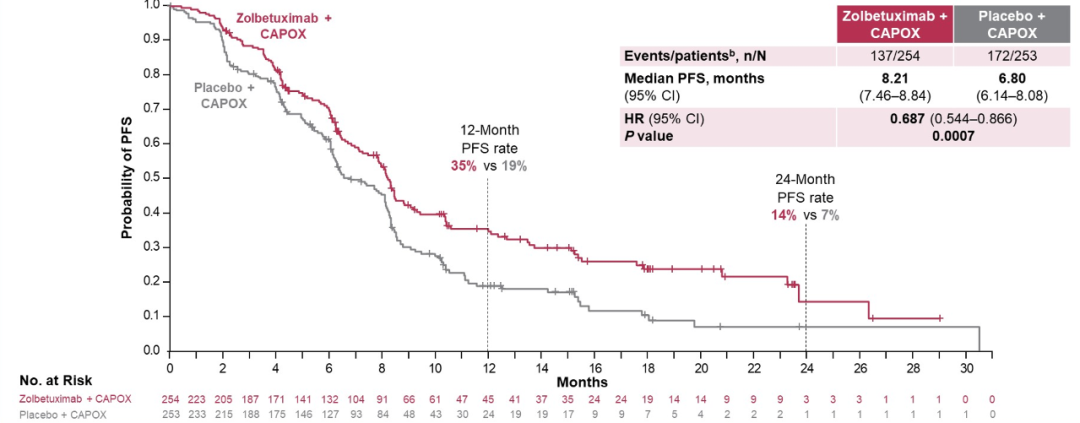
圖 2 GLOW 研究 PFS 數據
Zolbetuximab 聯合 CAPOX 組和安慰劑組的 mOS 分別為 14.39 個月 vs 12.16 個月(HR = 0.771;P = 0.0118)。
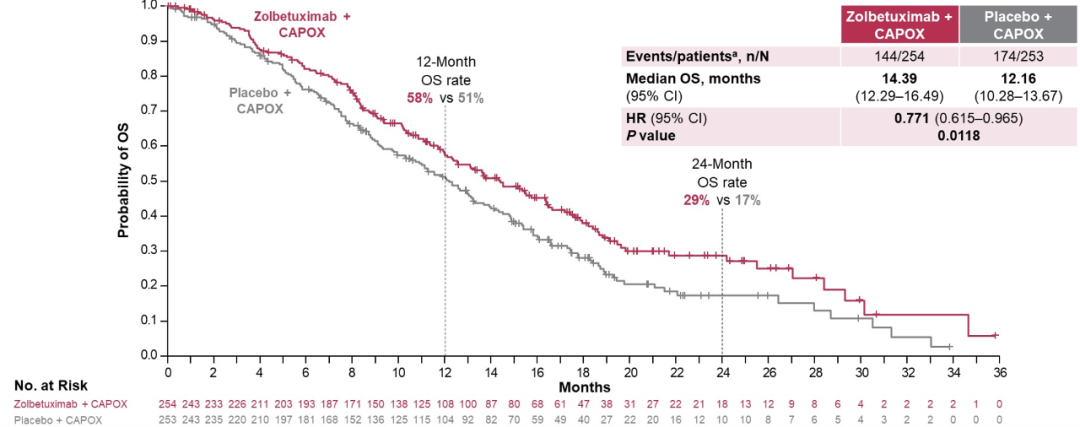
圖 3 GLOW 研究 OS 數據
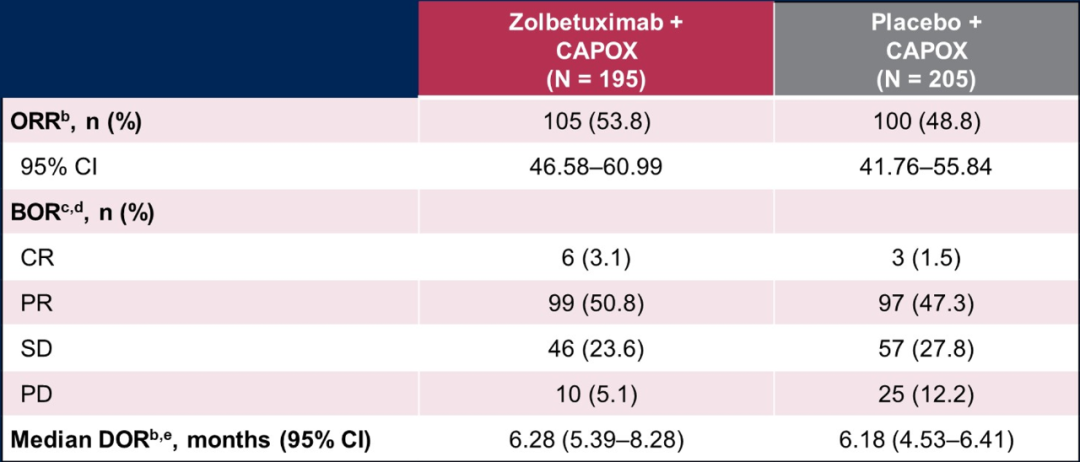
此外,在可測量病灶中,Zolbetuximab 聯合 CAPOX 和安慰劑組的客觀緩解率(ORR)分別為 53.8% vs 48.8%。
表 1 GLOW 研究的 ORR 數據
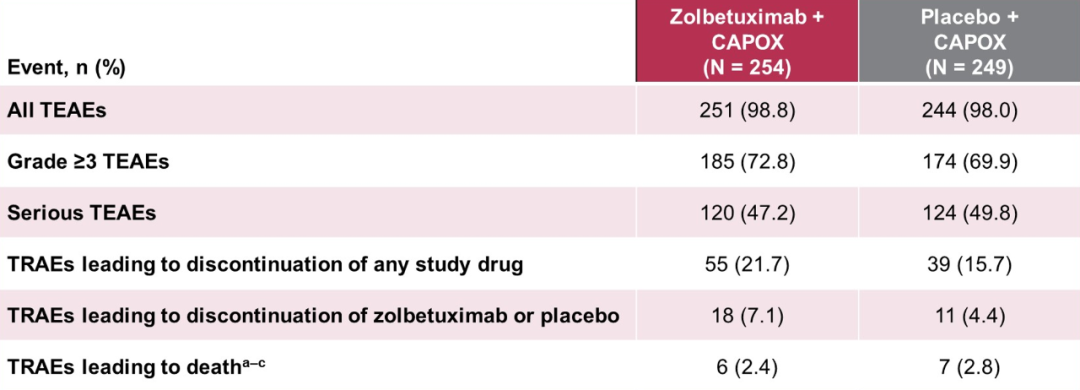
在安全性方面,兩組治療期間嚴重不良事件(TEAT)發生率相似,Zolbetuximab 聯合 CAPOX 組與安慰劑組分別為 47.2% vs 49.8%。Zolbetuximab 聯合 CAPOX 組最常見的不良事件是惡心、嘔吐和食欲下降。
表 2 所有治療患者不良事件
徐瑞華教授表示,本研究入組的患者均為 Claudin 18.2 陽性,即病理診斷中 70% 癌細胞可觀察到 Claudin 18.2 陽性。這一人群在晚期胃癌中大約占瞭 38%-43%。GLOW 研究的陽性結果意味著,Claudin 18.2 陽性的胃癌患者迎來瞭新的標準治療方案 —— 單克隆抗體聯合化療。由於該研究是全球多中心臨床研究,必然也能在全球晚期胃癌的標準治療有一席之地。
具成藥潛力的胃癌治療靶點
——Claudin 18.2
腫瘤分子靶向治療是以腫瘤細胞的標志性分子為靶點,通過有效的阻斷劑,幹預細胞發生癌變的環節 [3]。
理想的腫瘤分子靶向治療的靶點應具有以下特征 [4]:
① 是對惡性表型非常關鍵的大分子;
② 在重要的器官和組織中無明顯表達;
③ 具有生物相關性;
④ 能在臨床標本中重復檢測;
⑤ 與臨床結果具有明顯的相關性,當這些靶點受到幹預或抑制時,表達這類靶點的腫瘤患者絕大部分能取得有意義的臨床效果,而不表達此類靶點的患者則基本無效。
Claudin18.2 是較具臨床應用前景的靶點。一方面,Claudin 18.2 在消化系統腫瘤,尤其是胃癌、胰腺癌、膽道系統腫瘤以及部分結直腸癌中高表達,有較為廣泛的獲益人群。
另一方面,在正常生理狀態下,Claudin 18.2 僅在胃黏膜上已分化的上皮細胞中表達,而其他健康組織均無表達。
目前,各大藥企均佈局研發針對 Claudin 18.2 靶點的新藥。Zolbetuximab 是靶向 Claudin 18.2 的同類首創(first-in-class)單克隆抗體[2],通過抗體依賴細胞介導的細胞毒性作用(ADCC)和補體依賴的細胞毒性作用(CDC)起到抗腫瘤效果。此外,由於claudin18.2的高度特異性有助於T細胞識別腫瘤,因此也有很大潛力被用於嵌合抗原受體T細胞療法(CAR-T)。
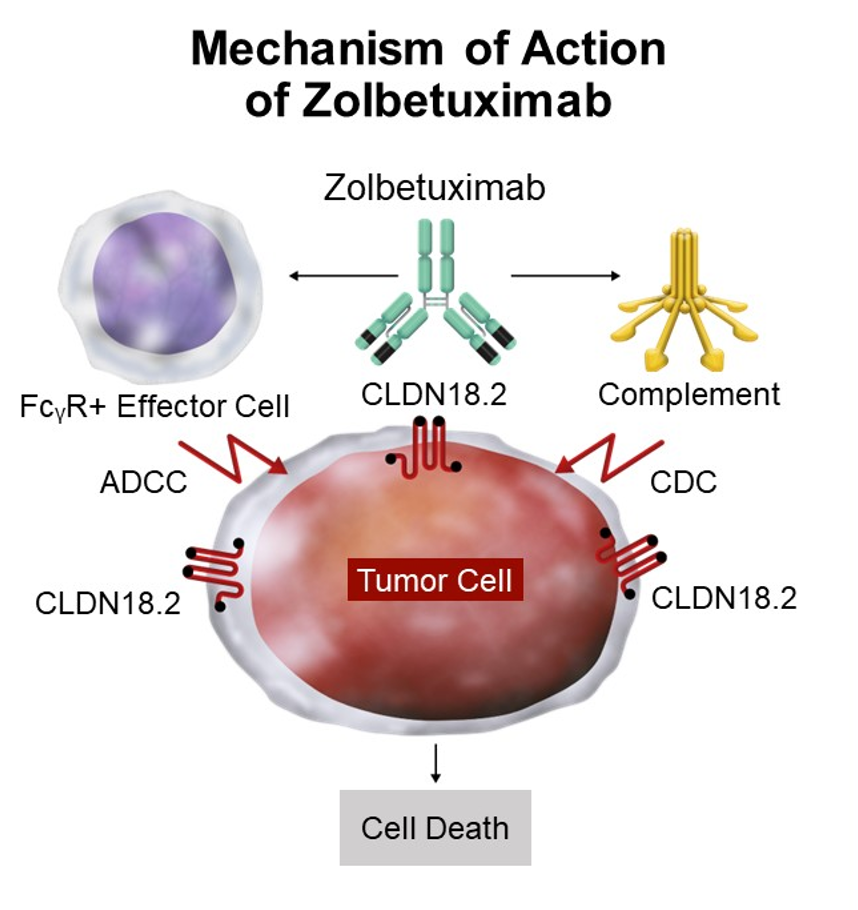
圖 4. Zolbetuximab 作用機制
徐瑞華教授表示,GLOW 研究的成功為 Claudin 18.2 靶點新藥研發打開瞭一扇大門,證明靶向 Claudin 18.2 的治療是可行的。而 first-in-calss 新藥 Zolbetuximab 的藥物結構和作用機制也會為後續的新藥研發提供啟示和借鑒樣本。
GLOW研究中亞洲患者占比較大,且PFS和OS亞組分析均顯示亞洲亞組接受Zolbetuximab+CAPOX治療的獲益尤為顯著。隨著 GLOW 研究的成功,相信 Zolbetuximab 會在世界各個國傢地區獲批上市,進入指南。Zolbetuximab 的獲益人群篩選、聯合治療方案也是將是未來探索方向。
作者:sweet;編輯:Huan




發表評論 取消回复