为积极推动我国临床肿瘤学事业的发展、提高临床肿瘤医师的临床与科研水平,进一步促进 CSCO 诊疗指南的制定和推广,2024 年 CSCO 指南大会于 4 月 26 日至 27 日在济南香格里拉大酒店举办。会议由中国临床肿瘤学会(CSCO)和北京市希思科临床肿瘤学研究基金会联合主办,最新版 CSCO 指南在本次会议发布。大会次日,丁香园肿瘤时间第一时间整理了肺癌(非小细胞肺癌/小细胞肺癌)指南更新情况,以飨读者。
非小细胞肺癌部分
早中期非小细胞肺癌篇
北京协和医学院 王志杰教授
更新一、分子分型部分更新
可手术 I-III 期 NSCLC
1.新增 I 级推荐:术后 II/III 期 NSCLC 进行 PD-L1 表达检测,指导辅助免疫治疗;
证据来源:
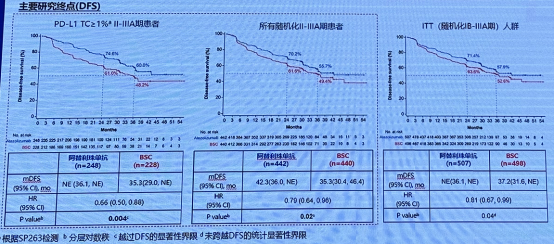
基于 IMpower010 研究的阿替利珠单抗于 2022 年 3 月 16 日获得 NMPA 批准,单药用于 PD-L1 阳性(TC ≥ 1%)、经手术切除、以铂类为基础化疗之后的 II-IIIA 期 NSCLC 患者的辅助治疗。
2.新增 II 级推荐:术后 II/III 期 NSCLC 进行 ALK 融合检测,指导辅助靶向治疗
不可手术 III 期及 IV 期 NSCLC
新增 II 级推荐:肿瘤组织进行免疫组化 MET 蛋白过表达检测
更新二、 IA、IB 期 NSCLC 的治疗部分更新
不可手术 IA、IB 期 NSCLC 的治疗部分:新增 II 级推荐:SABR 联合免疫治疗
证据来源:
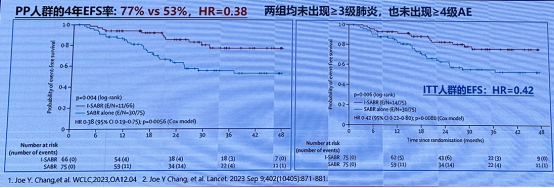
SABR+纳武利尤单抗 vs. SABR 用于早期或孤立性复发 NSCLC 的随机对照、II 期研究结果显示:SABR 联合免疫治疗相较于 SABR 显著提升了早期或孤立性复发 NSCLC 患者的 4 年 EFS 率,且安全性可控。
更新三、IIA、IIB 期 NSCLC 的治疗部分更新
1.新增 II 级推荐:根治性手术且术后检测为 ALK 融合患者,术后阿来替尼辅助治疗
证据来源:
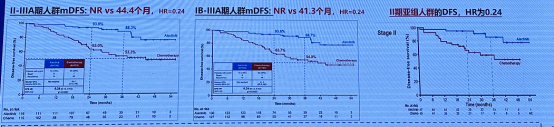
ALINA 研究期中分析:阿来替尼 vs. 化疗术后辅助治疗可切除 IB-IIIA 期 ALK+NSCLC,可切除 IB-IIIA 期 ALK + NSCLC 术后阿来替尼对比化疗辅助治疗显著改善了 DFS,该适应症于 2023 年 11 月 30 日获得 CDE 受理。
2.新增 II 级推荐:含铂化疗联合帕博利珠单抗/替雷利珠单抗新辅助 + 辅助治疗
证据来源:
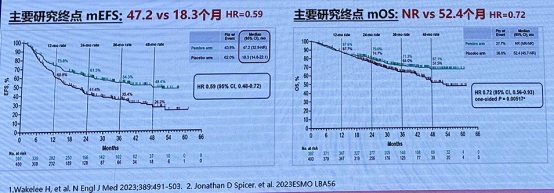
KEYNOTE-671:帕博利珠单抗 + 化疗 vs.化疗用于 II-IIIB 期 NSCLC 围术期治疗的 III 期研究,结果显示帕博利珠单抗组能够显著改善患者的 OS(NR vs 52.4 个月,HR=0.72,P=0.00517),显著提高 mEFS(47.2 个月 vs.18.3 个月,HR=0.59,95% CI 0.48-0.72)。FDA 于 2023 年 10 月 16 日批准帕博利珠单抗联合化疗新辅助治疗可切除(T≥4cm 或 N+)NSCLC、并在术后作为单药辅助治疗。
证据来源:
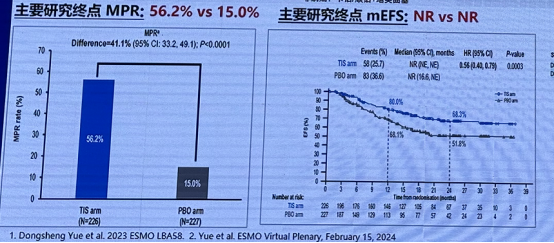
RATIONALE-315 研究:替雷利珠单抗 + 化疗用于可切除 II-IIIA 期 NSCLC 围术期治疗的 III 期研究,研究提示替雷利珠单抗联合化疗新辅助能够显著提高可切除 II-IIIA 期 NSCLC 患者的 MPR 与 pCR 率。该适应症于 2024 年 1 月 19 日获得 CDE 受理。
3.新增 III 级推荐:含铂化疗联合度伐利尤单抗新辅助 + 辅助治疗
证据来源:
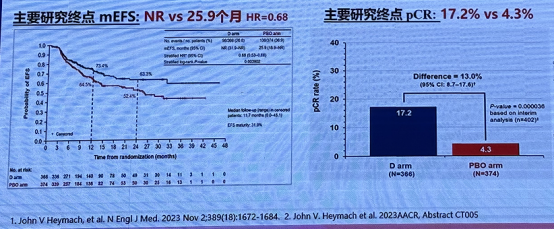
AEGEAN 研究:度伐利尤单抗 + 化疗 vs.化疗用于 IIA-IIIB 期 NSCLC 围术期治疗的 III 期研究,研究提示度伐利尤单抗联合化疗新辅助 + 度伐利尤单抗辅助治疗能够显著提高可切除 II-IIIA 期 NSCLC 患者的 pCR 率与 EFS率。
4.新增 III 级推荐:新辅助含铂化疗联合纳武利尤单抗治疗后的纳武利尤单抗辅助治疗
证据来源:
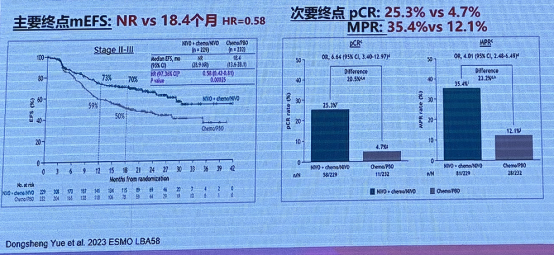
CheckMate 77T 研究:纳武利尤单抗 + 化疗 vs.化疗用于可切除 II-IIIB 期 NSCLC 围术期治疗的 III 期研究,研究期中分析提示新辅助纳武利尤单抗 + 化疗 + 纳武利尤单抗辅助治疗显著改善 IIA-IIIB 期NSCLC患者的 EFS。
更新四、可手术 IIIA 或 IIIB(T3N2M0)期 NSCLC 的治疗部分更新
1.新增 I 级推荐:含铂化疗联合特瑞普利单抗新辅助 + 辅助治疗
证据来源:

Neotorch 研究:特瑞普利单抗 + 化疗 vs. 化疗用于 II-III 期可切除的 NSCLC 围手术期治疗的 III 期研究,研究结果显示特瑞普利单抗组 pCR 提升 25 倍和 MPR 提升 6 倍的显著优势,且已经观察到 OS 数据的获益趋势。基于 Neotorch 研究,NMPA 于 2023 年 12 月 26 日批准特瑞普利单抗联合化疗围术期治疗后特瑞普利单抗单药辅助治疗可切除 IIIA-IIIB 期 NSCLC 成人患者。
2.新增 II 级推荐:含铂化疗联合帕博利珠单抗或替雷利珠单抗或卡瑞利珠单抗新辅助 + 辅助治疗
证据来源:
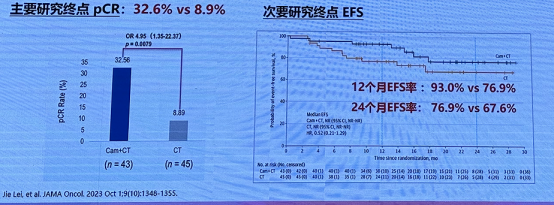
帕博利珠单抗或替雷利珠单抗见上文 KEYNOTE-671 和 RATIONALE-315 研究;
TD-FOREKNOW 研究:卡瑞利珠单抗 + 化疗 vs. 化疗新辅助治疗 IIIA/IIIB (T3N2)期 NSCLC 的随机对照 II 期研究,结果显示在 III 期可切除 NSCLC 患者中,卡瑞利珠单抗联合化疗显著提升 pCR 率,成为潜在的治疗选择。
3.新增 II 级推荐:根治性手术且术后检测为 ALK 融合患者,术后阿来替尼辅助治疗
证据来源:见上文 ALINA 研究;
4.新增III级推荐:含铂化疗联合度伐利尤单抗新辅助 + 辅助治疗
证据来源:见上文 AEGEAN 研究;
5.新增 III 级推荐:新辅助含铂化疗联合纳武利尤单抗治疗后的纳武利尤单抗辅助治疗
证据来源:见上文 CheckMate 77T 研究;
晚期非小细胞肺癌篇
上海市肺科医院 任胜祥教授
更新一、基因驱动阳性 NSCLC
EGFR 突变:
敏感突变
1.一线治疗新增I级推荐:贝福替尼
证据来源:

IBIO-103:贝福替尼 vs. 埃克替尼的 III 期临床研究,结果显示,贝福替尼组的由独立审查委员会评估的中位无进展生存期为 22.1 个月,埃克替尼组为 13.8 个月。贝福替尼于 2023 年 10 月 12 日被 NMPA 批准用于 EGFR 外显子 19 缺失或外显子 21L858R 置换突变的局部晚期或转移性 NSCLC 成人患者的一线治疗。
2.一线治疗新增II级推荐:奥希替尼联合化疗
证据来源:
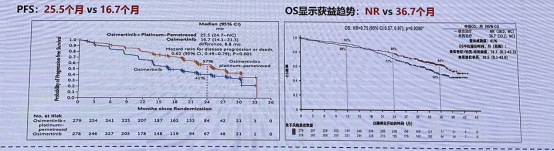
FLAURA2:奥希替尼 + 化疗 vs. 奥希替尼的 III 期临床研究,研究结果显示奥希替尼联合化疗组的 PFS 取得显著性获益,OS 显示出获益趋势。基于此研究,奥希替尼 + 铂类化疗于 2024 年 2 月 16 日被 FDA 批准用于 EGFR 19 Del/L858R 突变的局部晚期或转移性 NSCLC 患者的一线治疗。
3.二线治疗新增I级推荐: 贝福替尼
证据来源:

IBIO-102 研究:贝福替尼治疗一/二代 EGFR-TKI 耐药后 T790M 突变 NSCLC,最终的 OS 结果分析发现贝福替尼高剂量组的中位 OS 高达 31.5 个⽉。2023 年 5 月 31 日 NMPA 获批用于治疗既往接受 EGFR-TKI 耐药后产生 T790M 突变的局部晚期或转移性 NSCLC。
4. Amivantamab + Lazertinib 写入文字描述部分
证据来源:
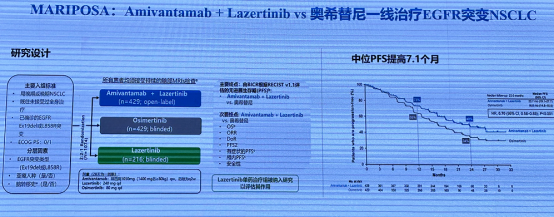
MARIPOSA 研究:Amivantamab + Lazertinib vs. 奥希替尼一线治疗EGFR 突变NSCLC,结果显示 Amivantamab 联合 Lazertinib vs. 奥希替尼显著改善一线 EGFR 突变晚期 NSCLC 患者的 PFS(HR,0.70;P<0 OS显示出良好获益趋势(HR,0.80;P=0.11)。>
5. BL-B01D1(EGFRXHER3-ADC)后线治疗写入文字描述部分
证据来源:
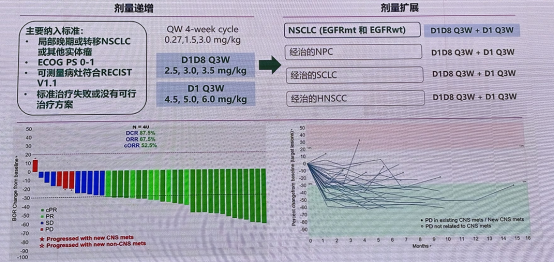
BL-B01D1 为基于双特异性拓扑异构酶抑制剂的 ADC,可同时靶向作用于表皮生长因子受体和人表皮生长因子受体 3(EGFR×HER3),早期的临床研究显示出一定的疗效。
ex20ins突变一线治疗:
1.新增 III 级推荐:Amivantamab 联合含铂双药化疗
证据来源:

PAPILLON:Amivantamab + 化疗 vs 化疗的 III 期临床研究,研究结果显示 Amivantamab 联合化疗的 PFS 和 ORR 显著优于化疗组。基于此,Amivantamab 联合卡铂 + 培美曲塞于 2024 年 3 月 1 日获 FDA 批准用于一线治疗 EGFR 20 号外显子插入突变的局部晚期或转移性 NSCLC(EGFR ex20ins突变晚期 NSCLC 的首个一线靶向疗法)。
2.新增 I 级推荐:舒沃替尼
证据来源:

WU-KONG 6:舒沃替尼治疗 EGFR 20 外显子插入突变的 NSCLC 的 II 期临床研究,该研究显示,舒沃替尼在 ORR 和 OS 方面展现出良好的疗效。基于此,2023 年 8 月 23 日获 NMPA 批准,舒沃替尼用于既往经含铂化疗出现疾病进展,或不耐受含铂化疗,且经检测确认存在 EGFR 20 外显子插入突变的局部晚期或转移性 NSCLC 患者。
3.后线治疗:取消「莫博赛替尼」推荐意见
ALK 融合阳性:
1)一线治疗优先推荐:阿来替尼、布格替尼、洛拉替尼;
2)一线治疗新增I级推荐:伊鲁阿克
证据来源:

INSPIRE 研究:伊鲁阿克 vs. 克唑替尼的随机 III 期研究结果显示,伊鲁阿克在 PFS 方面展现出显著性的获益,伊鲁阿克于 2024 年 1 月 16 日获 NMPA 批准用于 ALK 阳性局部晚期或转移性非小细胞肺癌的一线治疗。
3)新增克唑替尼耐药后I级推荐:伊鲁阿克
证据来源:
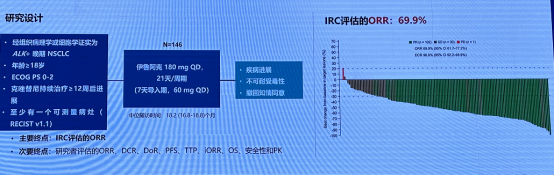
INTELLECT:伊鲁阿克治疗克唑替尼耐药的 ALK 阳性晚期 NSCLC 的 II 期研究,结果显示 IRC 评估的 ORR:69.9%,伊鲁阿克于 2023 年 6 月 28 日获得 NMPA 批准用于既往接受过克唑替尼治疗后疾病进展或对克唑替尼不耐受的 ALK 阳性局部晚期或转移性 NSCLC。
4)依奉阿克一线写入文字描述部分
证据来源:
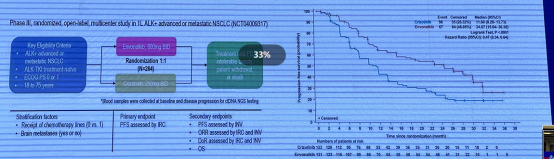
依奉阿克 vs.克唑替尼一线治疗 ALK 阳性 NSCLC 研究结果显示,依奉阿克对比克唑替尼延长了独立评审委员会(IRC)评估的 PFS,其上市申请已获 CDE 受理。
ROS1 融合:
1.一线和后线治疗新增 III 级推荐:Repotrectinib
证据来源:
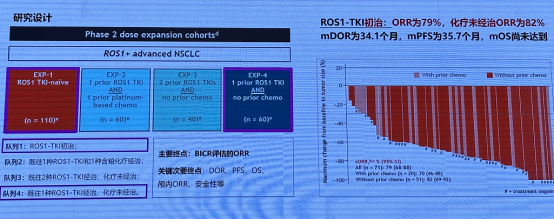
TRIDENT-1 研究 队列 1:Repotrectinib 治疗 ROS1-TKI 初治局晚期或转移性NSCLC 显示出一定的疗效。
证据来源:
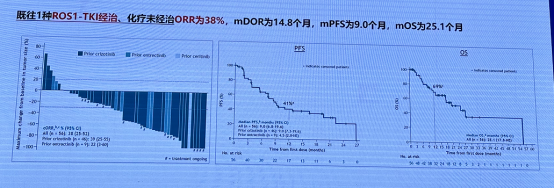
TRIDENT-1 研究 队列 4:Repotrectinib 治疗既往 1 种 ROS1-TKI 经治、化疗未经治 ORR 为 38%,mDOR 为 14.8 个月,mPFS 为 9.0 个月,mOS 为 25.1 个月。Repotrectinib 于 2023 年 5 月 10 日被 CDE 纳入优先审评审批,并于 2023 年 11 月 15 日获 FDA 批准用于治疗 ROS1 阳性的局部晚期或转移性 NSCLC 成人患者。
2. 安奈克替尼纳入文字描述部分
证据来源:
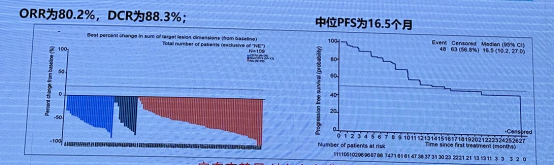
安奈克替尼在后线治疗 ROS1 阳性 NSCLC 中的 I/II 期研究中展现出良好的疗效与安全性。
MET 14 外显子跳突一线治疗和后线治疗:
1.上调「 特泊替尼 」为 I 级推荐
证据来源:
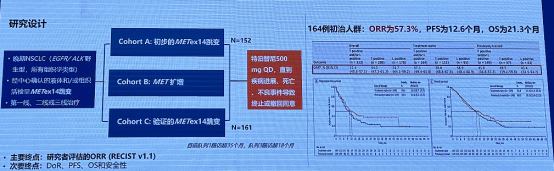
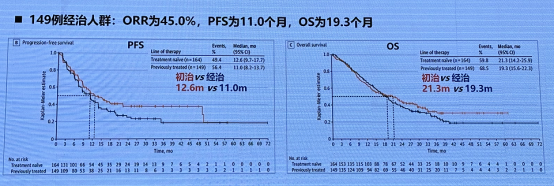
基于 VISION:特泊替尼治疗 MET 14 外显子跳变 NSCLC 的 II 期研究,该研究显示,特泊替尼治疗 MET 14 外显子跳变 NSCLC 一线和后线均展示出良好的疗效,特泊替尼于 2021 年 2 月 3 日获 FDA 加速批准,2023 年 12 月 5 日获得 NMPA 批准用于治疗 MET14 外显子跳跃突变的晚期或转移性NSCLC。
2.新增 I 级推荐:谷美替尼、伯瑞替尼
3.一线治疗新增II级推荐: 赛沃替尼
证据来源:

赛沃替尼治疗 MET 14 外显子跳跃突变 NSCLC 的 IIIb 期临床研究展现出良好的疗效,赛沃替尼治疗 MET 14 外显子跳突的局部晚期或转移性非小细胞肺癌的上市申请已获 NMPA 受理。
BRAF V600 突变 NSCLC:
新增 III 级推荐: Encorafenib + Binimetinib
证据来源:

PHAROS: Encorafenib+Binimetinib 治疗 BRAF V600E 突变 NSCLC 的 II 期研究结果显示,初治患者的 ORR 为 75%,59%的患者至少 12 个月时缓解,既往接受过治疗患者的 ORR 为 46%,33%的患者至少为 12 个月时缓解。Encorafenib 联合 Binimetinib 于 2023 年 10 月 11 日获 FDA 批准用于治疗 BRAF V600E 突变的转移性 NSCLC 患者。
RET 融合一线:
1.塞普替尼的 I 级推荐的证据类型由 3 类改为 1 类
证据来源:
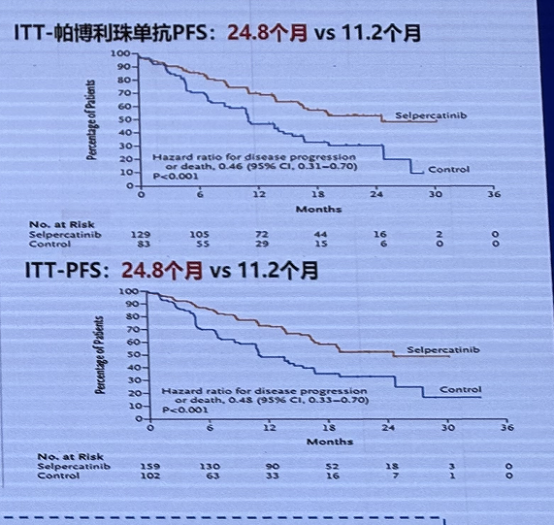
LIBRETTO-431:塞普替尼 vs. 帕博利珠单抗 + 化疗的 III 期研究,结果显示塞普替尼一线PFS较对照组翻倍。基于此,塞普替尼于 2022 年 9 月 30 日获 NMPA 附条件批准用于治疗 RET 基因融合阳性 NSCLC 患者,LIBRETTO-431 研究达到主要终点,进一步证实塞普替尼一线治疗的疗效。
2.上调「普拉替尼」为 I 级推荐
证据来源:
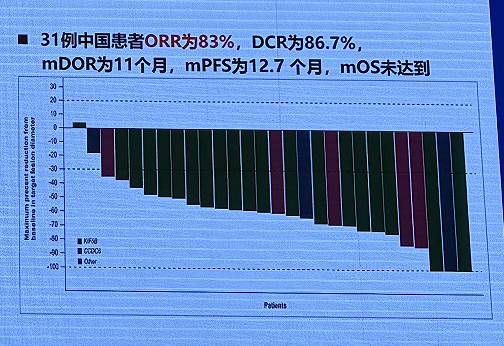
ARROW 中国队列数据更新:普拉替尼一线治疗 RET 融合阳性 NSCLC 展现出良好的疗效,普拉替尼于 2023 年 8 月 9 日获 FDA 常规批准,ARROW 研究中国人群数据提示普拉替尼在一线 RET 阳性患者中具有良好的抗肿瘤活性,普拉替尼于 2023 年 6 月 26 日获 NMPA 批准用于 RET 基因融合阳性 NSCLC 成人患者的一线治疗。
HER-2 突变后线:
上调「 德曲妥珠单抗 」为 II 级推荐
证据来源:
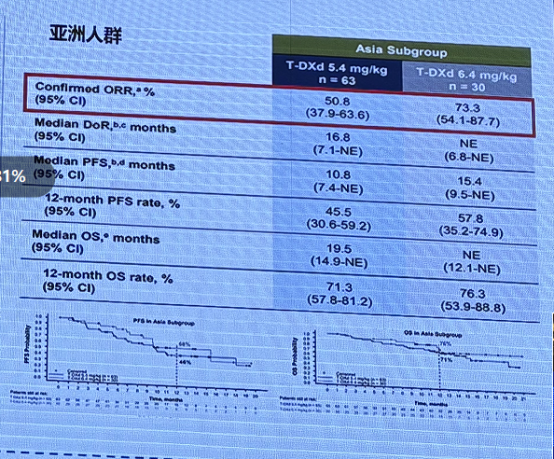
DESTINY-Lung02 亚洲人群数据:德曲妥珠单抗治疗 HER-2 突变 NSCLC的研究显示,DESTINY-Lung02 研究亚洲人群 ORR 分别为 50.8%和 73.3%,与全人群获益趋势一致。德曲妥珠单抗于 2022 年 8 月 11 日获 FDA 加速批准用于治疗既往接受过全身治疗的不可切除或转移性 HER2 突变 NSCLC,于 2024 年 1 月 3 日获 CDE 授予突破性治疗药物认定。
KRASG12C 小分子抑制剂:
新增:Garsorasib (D-1553)、IBI351、JDQ443 等文字描述部分
更新二、无驱动基因晚期 NSCLC
1.非鳞癌一线 PS=2 部分新增 II 级推荐:阿替利珠单抗
证据来源:
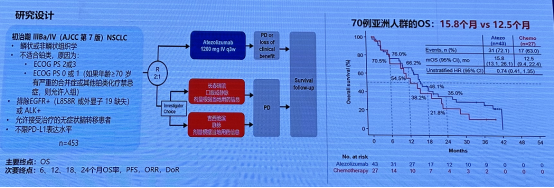
IPSOS 亚洲人群分析:阿替利珠单抗 vs. 单药化疗一线治疗不适合含铂化疗 NSCLC 患者的 III 期研究,IPSOS 亚洲人群 PS ≥ 2 占 82.9%,阿替利珠单抗单药对比化疗与全球 ITT 人群的 OS 和安全性一致,对于 PS=2 分的患者带来生存获益。
2.非鳞癌 Dato-DXd 二线治疗写入文字描述部分
证据来源:
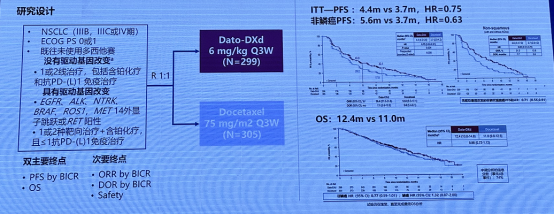
TROPION-lung01 : Dato-DXd vs. 多西他赛治疗经治 NSCLC 的 III 期研究中,Dato-DXd 展现出较好的疗效。
3.鳞癌一线 PS=2 部分新增II级推荐:新增阿替利珠单抗
证据来源:见上文 IPSOS 亚洲人群分析
小细胞肺癌部分
内科治疗篇
吉林省肿瘤医院 柳影教授
更新一、广泛期 SCLC 一线治疗
1.新增 III 级推荐:替雷利珠单抗 + 卡铂或顺铂 + 依托泊苷 4 周期后替雷利珠单抗维持治疗(III 级推荐,1A 类)
证据来源:
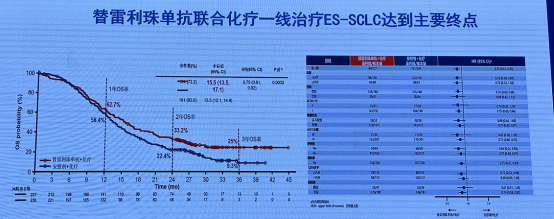
RATIONALE-312:替雷利珠单抗或安慰剂联合化疗一线治疗 ES-SCLC 的随机、双盲、安慰剂对照、多中心 III 期临床试验,替雷利珠单抗在 OS、PFS 及安全性方面均表现优异并达到主要终点(OS)。2023 年 10 月 18 日,NMPA 已受理替雷利珠单抗联合依托泊苷和铂类化疗用于一线治疗广泛期小细胞肺癌(ES-SCLC)患者的新适应症上市许可申请 。
2.新增 III 级推荐:特瑞普利单抗 + 卡铂或顺铂 + 依托泊苷 4 - 6 周期后特瑞普利单抗维持治疗(III 级推荐,1A类)
证据来源:
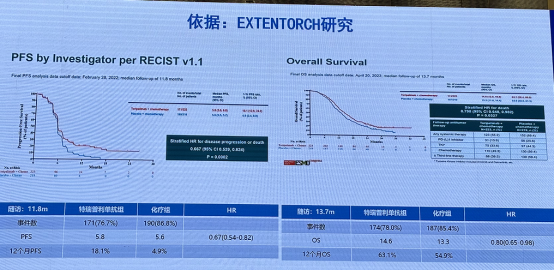
EXTENTORCH 研究:一项随机、双盲、安慰剂对照的多中心 III 期研究,评估特瑞普利单抗联合化疗对比安慰剂联合化疗一线治疗广泛期小细胞肺癌的疗效和安全性。特瑞普利单抗在 PFS 和 OS 均展现出显著性的获益,其安全性可。基于此研究,特瑞普利单抗用于治疗 ES-SCLC 获得 FDA 授予的孤儿药资格认定。2023 年 7 月,特瑞普利单抗基于 EXTENTORCH 研究的新适应症上市申请已获得 NMPA 受理。
3.新增注释:ETER701 研究结果
证据来源:
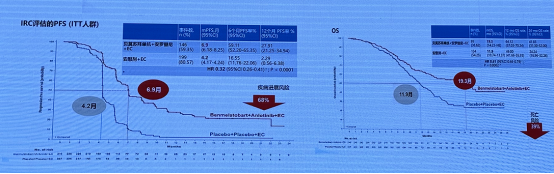
安罗替尼 + 贝莫苏拜单抗 + 化疗一线治疗 ES-SCLC 的 ETER701 研究结果显示,中位随访 14.0 个月,贝莫苏拜单抗 + 安罗替尼 + EC 组(n=246)和安慰剂 + 安慰剂 + EC 组(n=247)的 mPFS 分别为 6.9 和 4.2 个月(HR=0.32,95% CI:0.26-0.41,P<0 HR=0.61,95%CI:0.46-0.79,P>
4.新增注释:CAPSTONE-1 研究 3 年 OS
证据来源:
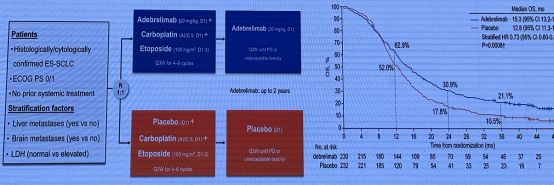
CAPSTONE-1 研究 3 年 OS 率达到了 21.1%,让 1/5 的患者生存期超过了 3 年。
5.新增注释:IMpower133 的扩展研究(IMbrella A)结果
证据来源:
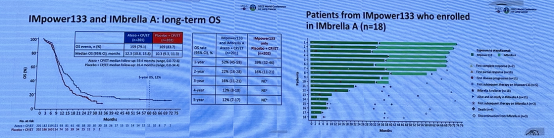
纳入了在 IMpower133 研究结束时继续接受阿替利珠单抗治疗或在 IMpower133 研究中停用阿替利珠单抗且处于生存期随访的 18 例患者,经过中位 59.4 个月的随访,阿替利珠单抗联合化疗 5 年的 OS 率达到 12%。
6.新增注释:ORINETAL 真实世界研究结果
证据来源:
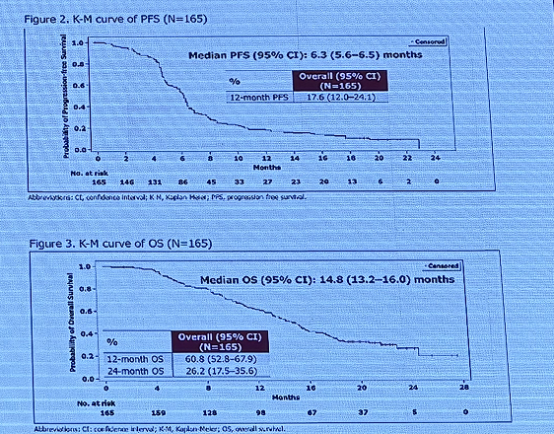
度伐利尤单抗联合化疗一线治疗中国广泛期 SCLC 真实世界 ORINETAL 研究结果:中位 PFS 达到 6.3 个月,中位 OS 达到 14.8 个月,12 个月 OS 率达到 60.8%,24 个月 OS 率达到 26.2%。
更新二、复发 SCLC 的治疗
注释部分更新:
1.芦比替丁联合免疫检查点药物
证据来源:
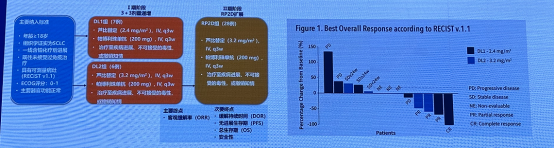
LUPER 研究 :芦比替丁联合帕博利珠单抗治疗复发 SCLC 的 I/II 期研究结果显示,ORR 为 46.4%,中位 DOR 为 2.99 个月,中位 PFS 为 5.3 个月(95% CI: 2.7-未达到),中位 OS 为 11.1 个月(95% CI:6.9-未达到)。
2.针对肿瘤细胞的 DLL3 抗体和 T 细胞的 CD3 的双特异性 T 细胞连接器 Tarlatamab 治疗复发 SCLC
证据来源:

DeLLphi-301 研究(Tarlatamab 治疗复发小细胞肺癌的 2 期研究)结果显示 Tarlatamab 在 PFS 和 ORR 有一定的疗效,2023 年 12 月 13 日,FDA 已接受 tarlatamab 上市许可申请,并授予优先审查权,可能成为复发小细胞肺癌治疗的突破口。
3.靶向 B7-H3 (CD276)的抗体偶联药物 DS-7300
4.靶向 PD-L1/VEGF-A 双特异性抗体 PM8002 联合紫杉醇治疗复发 SCLC
证据来源:
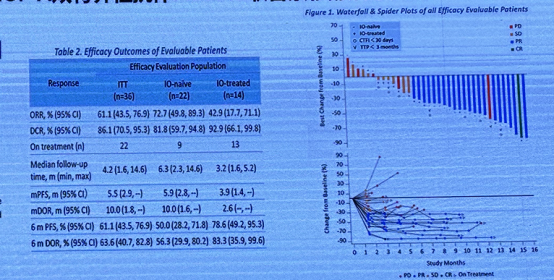
靶向 PD-L1/VEGF-A 双特异性抗体 PM8002 联合紫杉醇治疗复发 SCLC 的 2 期研究结果显示,PM8002 联合紫杉醇对复发小细胞肺癌具有良好的耐受性,毒性容易管理,尤其是对于经过免疫治疗的患者。
5.B和T淋巴细胞衰减因子(BTLA)抑制剂 Tifcemalimab 联合特瑞普利单抗
证据来源:
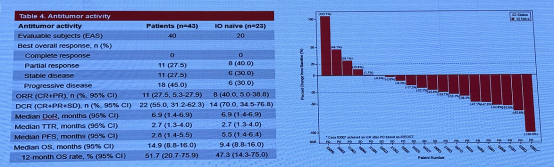
BTLA 抑制剂 Tifcemalimab 联合特瑞普利单抗 I/II 期研究结果显示,对于难治性 ES-SCLC 患者,tifcemalimab 联合特瑞普利单抗的耐受性良好。
更新三、曲拉西利推荐/证据提升
1.广泛期 SCLC一线治疗:曲拉西利或 G-CSF(含铂化疗±免疫检查点抑制剂前预防应用)(II 推荐,2A 类) 修改为 I 级推荐 1A 类
2.曲拉西利治疗复发 SCLC 的证据类别由 2A 类修改为 1A 类
证据来源:

TRACES 研究:曲拉西利在接受卡铂联合依托泊苷或拓扑替康治疗的中国广泛期 SCLC 患者的 Ⅲ 期研究。
研究证实化疗前给予曲拉西利可显著缩短第 1 周期严重中性粒细胞减少(SN)持续时间,显著降低 SN 的发生率,还可以减少发热性中性粒细胞降低(FN)的发生率和 3-4 级血液学毒性的发生率。
2023 年 10 月 30 日,NMPA 对曲拉西利从附条件批准转为常规批准,用于既往未接受过系统性化疗的广泛期小细胞肺癌患者,在接受含铂类药物联合依托泊苷方案治疗前给药,以降低化疗引起的骨髓抑制的发生率。
2023 年 8 月 14 日,NMPA 受理曲拉西利用于广泛期小细胞肺癌(ES-SCLC)患者,在接受含拓扑替康方案治疗前给药,以降低化疗引起的骨髓抑制的新适应症上市申请。
更新四、支气管肺/胸腺神经内分泌肿瘤的治疗
「 度伐利尤单抗联合曲美木单抗 」作为远处转移性支气管肺/胸腺神经内分泌肿瘤(典型类癌和不典型类癌)后线治疗的 III 级推荐
证据来源:
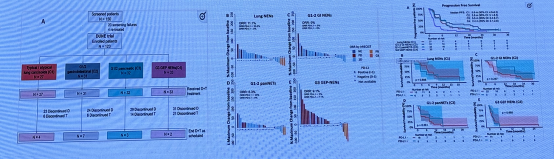
DUNE 研究:度伐利尤单抗联合曲美木单抗治疗进展期胃肠胰腺和肺来源的典型/不典型类癌的单臂、多中心、II期临床研究结果显示,纳入 27 例经标准治疗失败后的进展期典型/不典型肺类癌患者,有效率达 11.1%,其中 PD-L1(+)患者ORR 可达 33.3%,PD-L1(-)患者未看到治疗反应。中位 PFS 为 5.6 个月(95%CI:4.9-6.2),可作为该类进展期患者后线治疗的选择之一。
放射治疗篇
中国医学科学院肿瘤医院 毕楠教授
更新一、局限期 SCLC 的初始治疗
注释部分中增加如下描述:
近期随机对照 II 期研究和回顾性研究显示,如果可以安全地给予更高剂量(60Gy/40 次,1 天两次;65 Gy/26F 1 天一次;或肿瘤同步加量至 54Gy/30 次,1 天两次),可能改善 OS 或 PFS。一项中国 Ⅲ 期随机对照临床研究(NCT 03214003)对比了高剂量(54Gy/30f/BID)和标准剂量(45Gy/30f/BID)两种超分割方案,初步结果显示高剂量超分割方案可延长 OS 和 PFS,正式结果尚未公布。
更新二、广泛期 SCLC 的一线治疗
胸部放疗Ⅱ级推荐(2A):在注释中标明:
1.化疗后有效的胸部巩固放疗可改善 OS。目前,一线化疗 + 免疫治疗是广泛期 SCLC 的标准方案,如何联合放疗以及优化放疗剂量,有待深入研究与探索。
2.一项 I 期试验探索含铂化疗后胸部放疗 45Gy/15 次同步不同剂量帕博利珠单抗巩固维持治疗,结果显示联合治疗方案的安全性支持进一步研究;
3.另一项 1/2 期研究采用含铂化疗后胸部放疗 30Gy/10 次两周后序贯纳武利尤单抗和伊匹木单抗巩固维持,毒性与已知不良事件一致,尽管研究方案未显著改善 PFS,但发现肿瘤病灶中存在淋巴细胞浸润和迁移的患者最有可能改善愈后。
更新三、放疗并发症的处理
1.2 级放射性肺损伤新增 I 级推荐:布地奈德鼻喷雾剂
2.放射性食管炎调整部分语句和推荐(红色为调整部分):
I 级推荐 1 级:改变饮食,体位指导。可以使用氢氧化铝、氢氧化镁及黏膜表面保护剂如蒙脱石散、重组人表皮生长因子和硫糖铝混悬液等。
I 级推荐 2 - 4 级:应用以利多卡因、制霉菌素酌食糖皮质激素及庆大霉素为基础的混合液,配合口服镇痛药物;质子泵抑制剂可以抑制胃酸分泌对食管黏膜的损伤,减轻胸骨后烧灼感;钙离子拮抗剂可以缓解痉挛。发现细菌及真菌念珠菌感染会增加口服制霉菌素和氟康唑治疗 。
4 级考虑经皮胃造瘘置管营养或肠外营养。
II 级推荐:2 - 3 级新增食管镜检查。
内容整理:毛阳
编辑:Bree;题图:丁香园创意团队




發表評論 取消回复