本文作者:陸可馨
「希望上班第一天不要太忙啊。」
端午假期後的第一天,我早早坐在辦公室,一邊在心裡默默祈禱著,一邊打開電腦緩慢啟動自己的工作狀態。
「陸姐!你來啦!」師妹突然出現在我的背後。
「太陽打西邊出來瞭,你怎麼來的比我還早?」我調侃道。
「別提瞭陸姐。」師妹露出一張苦瓜臉,「昨晚被喊回來加班加到現在的,還記得咱們心內科『常客』丁大爺不?」
「怎麼回事?」我頓時覺得有些不妙。
丁大爺是市裡某個科研院所的退休工程師,自打退休以來就在我們醫院的門診看病瞭。丁大爺平日裡談吐頗有學者風范,而且堅持十幾年風雨無阻地來醫院復查,一來二去,他也成為瞭我們口中的「模范病人」。
不僅如此,他還是我迄今為止見過病程最長的肥厚型心肌病患者——從 20 多歲確診,到如今 78 歲高齡,已經超過 50 年。
「丁大爺昨晚心衰被 120 送急診去瞭,急診推瞭速尿沒效果,後半夜轉進來住院瞭。」
「現在情況呢?」
「泵瞭米力農和新活素,沒啥大事瞭。」
雖然存在心力衰竭的情況,但丁大爺的生活質量一直還可以,近年來的病情也比較穩定。為什麼會突發心衰?問題到底有多嚴重?我暗自擔心著,點開瞭丁大爺本次入院的病程記錄。
01.
78 歲高齡,丁大爺的健康狀況一直也不簡單。
除瞭年輕時就確診的心肌病和高血壓,丁大爺的診斷中還包含冠心病、心律失常、腎功能不全、白內障和前列腺肥大等疾病。好在丁大爺和傢屬的依從性極高,這些疾病都得到瞭及時的診療和有效的控制。
不過,當我點開超聲心動圖報告時,卻有瞭一點出乎預料的發現。
「陸姐,我就是想問這個,一般的肥厚型心肌病是單純左心室肥厚對吧,為什麼這個的右室我看著也像增厚瞭呢?還有二尖瓣,也像有點增厚。」師妹率先發出疑問。
「也有的會同時在心尖處存在心肌肥厚[1],或者是心腔中部出現心肌病變[2]。」我回答道,「但你說的沒錯,像這樣同時雙心室室壁肥厚,還出現二尖瓣增厚的情況是極其罕見的。」
「看看他之前的心超就知道瞭。」師妹說著打開瞭另一臺電腦的門診病歷系統。我湊過去一看,她已經找到瞭丁大爺 10 年前在我院留下的第一份病例——這幾乎是我院最早電子化的第一批病歷瞭。
2013 年,丁大爺來到我科就診,抱怨走路後經常出現胸部不適和呼吸困難,小腿也開始浮腫起來。
接診醫生考慮到丁大爺的肥厚型心肌病病史,認為可能是疾病加重引起的癥狀,在丁大爺每天服用美托洛爾和氨氯地平的基礎上,又增開瞭依那普利每日服用,並囑咐丁大爺在水腫嚴重時吃一片復方阿米洛利。
第二份病例的時間是 2014 年。這次,丁大爺因為惡心、頭暈和胸部不適就診,心電圖發現瞭三度房室傳導阻滯和明顯的心動過緩,隨後入院接受手術,植入瞭一枚雙腔植入型心律轉復除顫器。
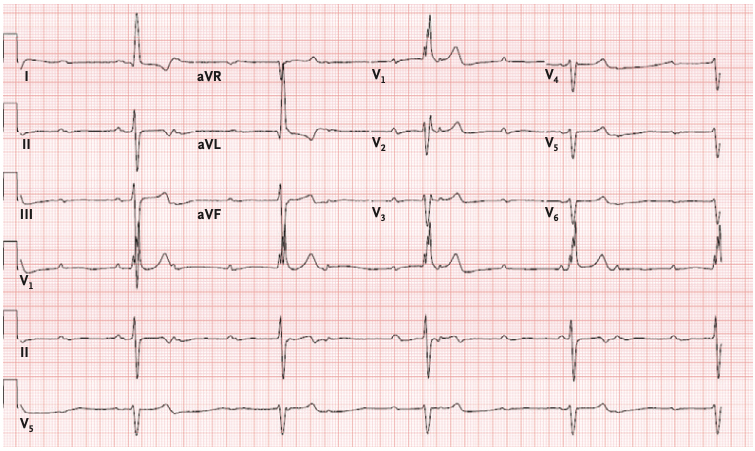
患者心電圖顯示房室傳導阻滯和心動過緩(圖源:參考資料 11)
「植入除顫器?這個時候丁大爺還沒有出現心動過速吧?」師妹再次感到不解。
「現在的除顫器大多數是帶有起搏功能的,對於丁大爺這種有致命性心律失常風險的心肌病患者來說,植入除顫器可比植入起搏器劃算太多瞭。」我說。
繼續看下去。手術後 4 個月,丁大爺出現瞭房顫,雖然第一次房顫復律成功,但 3 天後房顫復發,這次醫生開出瞭胺碘酮和華法林長期治療。
此後很長的一段時間,丁大爺雖然隔三差五來復診,但病歷基本上都是流水賬,他的心臟情況一直穩定得很,直到距今 2019 年的一次復診,丁大爺因「肺水腫」再次進瞭醫院。
「這個我記得!」師妹說,「當時我在跟老板門診,好像傢屬說是出去旅遊吃得太咸瞭還是怎麼的,總之利尿劑治療後就好轉瞭,基本沒什麼大的影響。」
不過,也正是這次就診後,丁大爺的心臟情況就逐漸開始走下坡路:一爬樓梯或者走斜坡就會出現呼吸困難、極度疲憊,晚上睡覺還經常需要枕兩個枕頭才能安穩入睡,更糟糕的是,復查時主任程控除顫器發現丁大爺存在間歇性的室性心動過速。
聯系到本次心超中不同尋常的表現,我和師妹都有瞭不妙的預感。
02.
醫生辦公室門外突然傳來一陣嘈雜,我回頭看去。
「實習生嗎?完瞭!今天入科來著,我還沒準備好 SP。」師妹趕緊跳起來。(SP,standard patient:標準化病人,用於醫學教育、醫療專業人員的評估。)
我沉思片刻:「正好,丁大爺和他傢人和我們科室都比較熟,配合度也高,你去問問,方便的話帶同學們練習病史詢問吧。」
一個多小時後,師妹帶著一群小孩兒浩浩蕩蕩地回到辦公室。
我和師妹快速交換眼神:咋樣?還不錯。
實習生就座後,一位男生主動站起來:「我們組派我做代表,整理瞭一下患者的病史。」我點頭示意他繼續講下去。
男生清瞭清嗓:「首先,丁爺爺的人生堪稱傳奇。」
我再次和師妹快速交換眼神:你教的?我不是,我沒有。
男生繼續講下去,時間回到 58 年前。
20 歲以前,丁大爺——或者應該說「小丁」——還沒有受到心臟疾病的困擾。那時,小丁不僅學習成績優秀,運動水平也一流,不僅是校田徑隊的成員,還在校運會上打破過百米短跑記錄。
然而,在 21 歲的某一天,小丁在校隊訓練突發小腿麻木刺痛。起初,他並沒有太當回事,但休整瞭一段時間後,癥狀不僅沒有減輕,他還發現自己腳上和腿上的出汗量明顯減少。然而,皮膚科的醫生也並沒有給出明確診斷,小丁的運動成績受到傷病影響一路下滑。
一次短跑訓練後,小丁突然感到頭暈難忍,被同學們送往醫院。也正是在這一次,他被心內科醫生首次診斷出肥厚型心肌病。好在當時,小丁的病情並不嚴重,除瞭不能再踏入自己熱愛的跑道,他還是順利的結婚生子。
隨著歲月增長,小丁逐漸變成「老丁」,疾病對身體的影響也越來越明顯。53 歲那年,老丁在單位體檢中被查出左心室肥大和高血壓,心超顯示左心室壁對稱性增厚至 19mm(正常值≤11mm),並同時存在二尖瓣增厚和二尖瓣反流。隨後,老丁開始常規服用治療心肌病的美托洛爾和治療高血壓的氨氯地平。
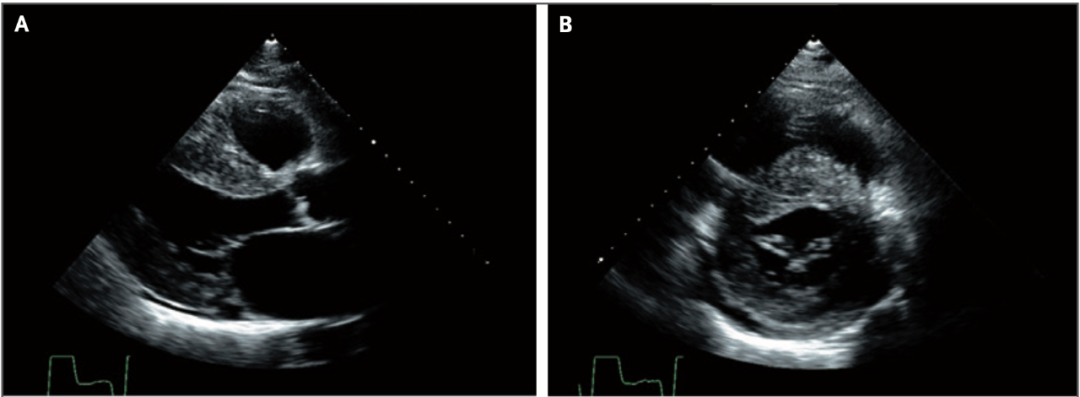
心超示心肌肥厚(圖源:參考資料 11)
此後多年,老丁的情況倒也一直穩定,直到退休後,已經成為「丁大爺」的他開始在離傢最近的我院定期復診……後面的故事,就是我們在門診系統裡看到的內容瞭。
03.
聽完實習生的病史匯報,我對其中幾個疑點陷入瞭沉思:
首先,是丁大爺 20 歲初曾經出現的腿部少汗、麻木刺痛癥狀,是下肢周圍神經病嗎?
其次,丁大爺的左心室肥厚和高血壓似乎是同時出現的,而且連續多次的心超檢查均未發現肥厚型心肌病中常見的左心室流出道梗阻,這又意味著什麼?
此外,在等待病史問詢的過程中,我又回顧瞭丁大爺近幾年的門診和住院檢驗報告記錄,發現他的肌酐和尿素氮水平逐步隱匿升高,截至這次住院,丁大爺已經發展成瞭伴白蛋白尿的輕度腎功能不全。
心臟傳導異常,雙心室壁增厚心肌病,周圍神經病,腎病......種種不尋常,是不同疾病的巧合嗎?不,我很快否定瞭這個念頭。無論患者有多少癥狀、多少異常體征,還是應該盡可能用一種疾病來穿起整個框架,這是「醫學一元論」的基本原則。
那麼,對於丁大爺的種種癥狀,什麼才是突破口?
「啊對瞭老師!剛剛忘記說傢族史。」匯報的男生打斷瞭我的思路,「根據患者和傢屬的描述,丁爺爺的姐姐、妹妹,以及他的外甥女也都患有肥厚型心肌病,而其他傢屬,包括兒子、兩個孫子都沒什麼大問題。」
我一下子頓住瞭:長達 58 年的肥厚型心肌病病史、長達 10 年的我科隨訪病史、我對患者的瞭解等等因素,讓我都陷入瞭慣性思維,反而忽略瞭最基本的問題……
04.
安頓好實習生的任務,師妹迅速回到電腦前:「陸姐,你是不是想到什麼瞭?」
我點點頭:「肥厚型心肌病是常染色體顯性遺傳[3],但是丁大爺這個傢族史很難不讓人在意。」
「傳男不傳女,X 連鎖遺傳?」師妹搶答道。
我點點頭:「但因為是老病人,在之前的門診隨訪中,我們很少關註到這點,患者也沒怎麼提過……結合他的癥狀,我目前想到瞭兩個可能。」
首先是淀粉樣變性。
湊巧的是,我前段時間剛剛參與瞭一例與內分泌科會診的遺傳性轉甲狀腺素蛋白淀粉樣變性,其緩慢溫和的病程可以解釋丁大爺的部分癥狀,但是,該病患者的胃腸道癥狀往往非常嚴重[4],而丁大爺沒有這方面的困擾;而更為兇險的免疫球蛋白輕鏈淀粉樣變性,患者生存期非常短[5],恐怕撐不到今天。
其次是溶酶體貯積病(LSD)。
如果考慮到可能的 X 連鎖遺傳,LSD 有三種符合標準:達農病、法佈雷病和黏多糖貯積癥 II 型[6]。
達農病患者雖然普遍存在類似於肥厚型心肌病的心臟表現,但該病的男性患者早至 12 歲即可發病,且幾乎均存在智力障礙和肌無力[7];黏多糖貯積癥 II 型患者則有典型的皮膚病變、中樞神經受累和面容異常[8]……
那麼,法佈雷病呢?
和其他 LSD 一樣,法佈雷病也是溶酶體內清除特定化合物的酶活性大幅降低或缺失,引起有毒化合物累積,從而損傷特定細胞和器官。
在法佈雷病患者中,溶酶體 α-半乳糖苷酶 A 的活性缺失導致酰基鞘鞍醇三己糖(Gb3)在多種細胞的溶酶體中蓄積,而 Gb3 蓄積後會進一步轉化為有毒的親水性去酰化衍生物,從而產生細胞毒性、促炎性和促纖維化等多種有害效應。
Gb3 常蓄積於自主神經節、後根神經節、腎小球、腎小管和腎間質細胞、心肌細胞、血管平滑肌細胞、角膜內血管內皮細胞和淋巴管內皮細胞、瓣膜纖維細胞和心臟傳導纖維。因此,法佈雷病主要累及外周神經系統、皮膚與毛細血管、眼部、腦血管、心臟(包括心臟瓣膜、心臟傳導系統和心肌)、腎臟等部位。
由於 Gb3 的蓄積、向有毒產物轉化和發揮細胞毒性的一系列過程在組織間存在差異,法佈雷病的癥狀通常隨年齡增長序貫出現。
「這樣看來,很有必要做個基因檢測瞭。」師妹總結道。
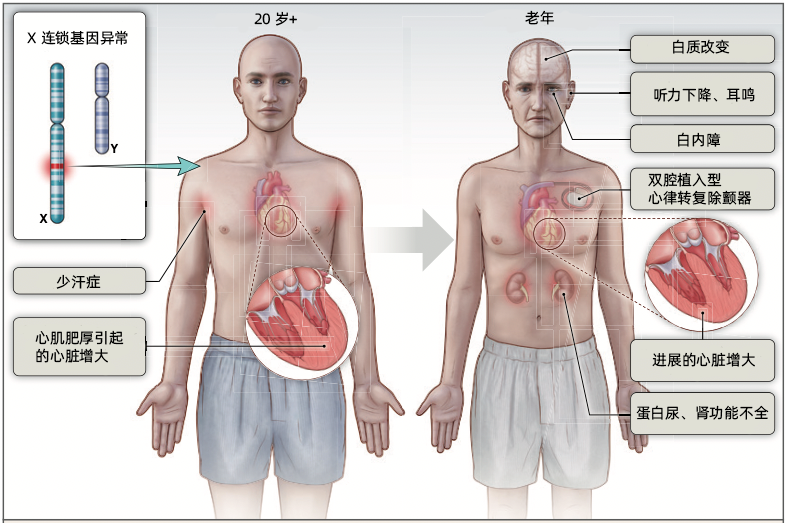
丁大爺癥狀示意圖(圖源:參考文獻 11 插圖編譯)
05.
在和丁大爺及傢屬進行溝通後,我們很快簽署瞭知情同意,並為丁大爺聯系瞭遺傳病檢測實驗室。
15 天後,我收到瞭實驗室傳來的兩份檢測報告。其中的基因檢測報告顯示,丁大爺的 GLA 基因(該基因編碼溶酶體 α-半乳糖苷酶 A)外顯子 6 上檢測到 R301G 突變,該突變已知可導致法佈雷病;另一份酶活性檢測報告顯示,丁大爺的血漿樣本中未檢測到 α-半乳糖苷酶 A 的殘留活性,證實丁大爺為經典型法佈雷病患者。
真相大白,我卻並沒有為此感到開心。
有近年研究顯示,在我國肥厚型心肌病患者中,法佈雷病的發生率約為 0.93%,這不是一個小數字。但由於癥狀多樣且缺乏特異性,法佈雷病依然經常被誤診和漏診。
相比治療手段有限的肥厚型心肌病,法佈雷病雖然累及全身多系統,但早就有瞭治療方案。
根據 2013 年的《中國法佈雷病(Fabry 病)診治專傢共識》,酶替代治療——即利用基因重組技術體外合成 α-Gal A 替代體內缺陷的酶——可以很大程度上減輕甚至避免心臟和腎臟的病變。
多個隨機對照及開放擴展臨床試驗結果均顯示重組人類 α-Gal A 替代治療法佈裡病可減少患者細胞內 GL3 的沉積,有效減輕患者的肢端疼痛、胃腸道癥狀,改善心肌肥厚,穩定腎功能,從而改善患者的生活質量和預後。
但是,對於丁大爺來說,這份真相來得有些太晚瞭。
《中國法佈雷病(Fabry 病)診治專傢共識》中提到,一般來說,法佈雷病的患者往往在兒童至青少年時期就出現臨床癥狀,並隨病程進展而逐漸加重,許多患者尤其是男性患者常在中青年死於嚴重的腎功能衰竭或心腦血管並發癥。
丁大爺這樣一位活到瞭 78 歲高齡的法佈雷病患者,實屬罕見。
但同樣,對於 78 歲高齡的丁大爺來說,心臟病已經進入瞭不可逆階段,雖說短期內不至於危及生命,但積極治療也無法逆轉病變。
更揪心的是,此前丁大爺為瞭治療房顫而服用的胺碘酮,可能通過在溶酶體中競爭性抑制磷脂酶 A2[10]而加速法佈雷病的進展,丁大爺的心肌病在房顫過後不斷加重,也不能完全排除與胺碘酮有關。
這個「救命」的藥物,實際上卻加重瞭他的癥狀。
好在,當開始懷疑法佈雷病的時候,我們已經第一時間為丁大爺暫停瞭胺碘酮的醫囑。經過和丁大爺及傢屬的溝通,我們為丁大爺調整治療方案,很快,他的病情穩定得以出院。未來,丁大爺的傢屬、後代也可以通過遺傳咨詢而避免法佈雷病的影響。
但我依然會想,在這段橫跨瞭 58 年的病程裡,在丁大爺隨訪的 10 年時間裡,如果有人能早一點察覺到蛛絲馬跡,那麼,結果是否會截然不同呢?(策劃:z_popeye|監制:carellero)
致謝:本文經 中山大學孫逸仙紀念醫院心血管內科副主任醫師 麥憬霆 專業審核




發表評論 取消回复