本文作者:二甲双胍
2018 年末,首都医科大学附属北京友谊医院肝脏移植中心来了两名素不相识的患者。
两个年轻的生命正饱受两种不同疾病的折磨,但同为肝脏移植中心的患者,他们也有着相似之处——肝脏无法正常处理体内特定的代谢产物,进而导致神经系统损害,甚至危及生命。
绝望笼罩,肝移植成为了唯一的生存希望。
他们还不知道,即将给他们带来奇迹的,是一台「世界首例」的肝移植手术。
不幸中的巧合
19 岁的小勇(化名)生于一个农村家庭,他和双胞胎弟弟均患有 OTCD(鸟氨酸氨甲酰基转移酶缺乏)和 HHH 综合征(高鸟氨酸血症-高氨血症-高同型瓜氨酸尿症)。
这是两种罕见的代谢性疾病,会引起肝脏的尿素循环功能障碍,轻者可以表现为轻微神经系统症状,但随着疾病进展,重者则可表现为严重的智力障碍、嗜睡、昏迷。
一次高蛋白饮食后,小勇的弟弟抢救无效去世。惨痛的经历为这个家庭敲响警钟,父母带着小勇四处求医,希望能找到一线生机。
而 9 岁的小航(化名)则在刚出现记忆力下降时,就被诊断为高蛋氨酸血症。这是一种蛋氨酸代谢障碍疾病,MRI 提示小航已经出现了脑白质的损伤,再进展下去,智力减退和神经损害会更加严重。
两个生命、两个家庭的不幸,却也同时面临着相似的困境。
肝移植是治疗两名患儿最好的方法,然而,小勇和小航都是 O 型血,这个血型的人往往可以作为器官供者提供给其他血型,但自身却无法接受其他血型的器官——这也意味着,两名患儿需要的肝源更加稀缺,传统器官的移植漫长等待,于他们而言更是遥不可及。
最后一线求生的希望,将两名患儿引到了同一个地方——北京友谊医院朱志军教授门诊。

「代谢缺陷疾病的一个特点就是,肝脏功能除了某一个酶缺乏的代谢缺陷以外,其他功能是正常的,比如合成蛋白质或凝血物质、胆红素代谢等都没有问题。」朱志军教授说。
朱志军教授介绍,在未来,这些代谢缺陷疾病都有可能通过基因治疗来解决。因此,大多数患者家庭更期待将肝脏移植作为一种「过渡」——避免再发生代谢失衡,同时又保留部分肝脏,等到数年以后基因治疗技术成熟,还有机会再接受治疗。
然而,这样的愿望在现阶段很难实现。
目前,代谢缺陷疾病肝移植意味着患者原本的「病肝」被彻底拿走,换着供者肝脏,长期服用免疫抑制药物生存。即使未来基因治疗技术成熟,这些已经失去了自己的肝脏的患者,也没有任何使用基因治疗的机会。
但小勇和小航的同时出现,成为了一种幸运的巧合。
虽然两人都患有代谢性疾病,但是产生损伤的机制上并没有交叉,加之两人血型相同,朱志军教授大胆提出了一项前所未有的手术方案:
将小勇和小航的部分肝脏互换移植,作为彼此代谢缺陷的补充,从而缓解疾病!
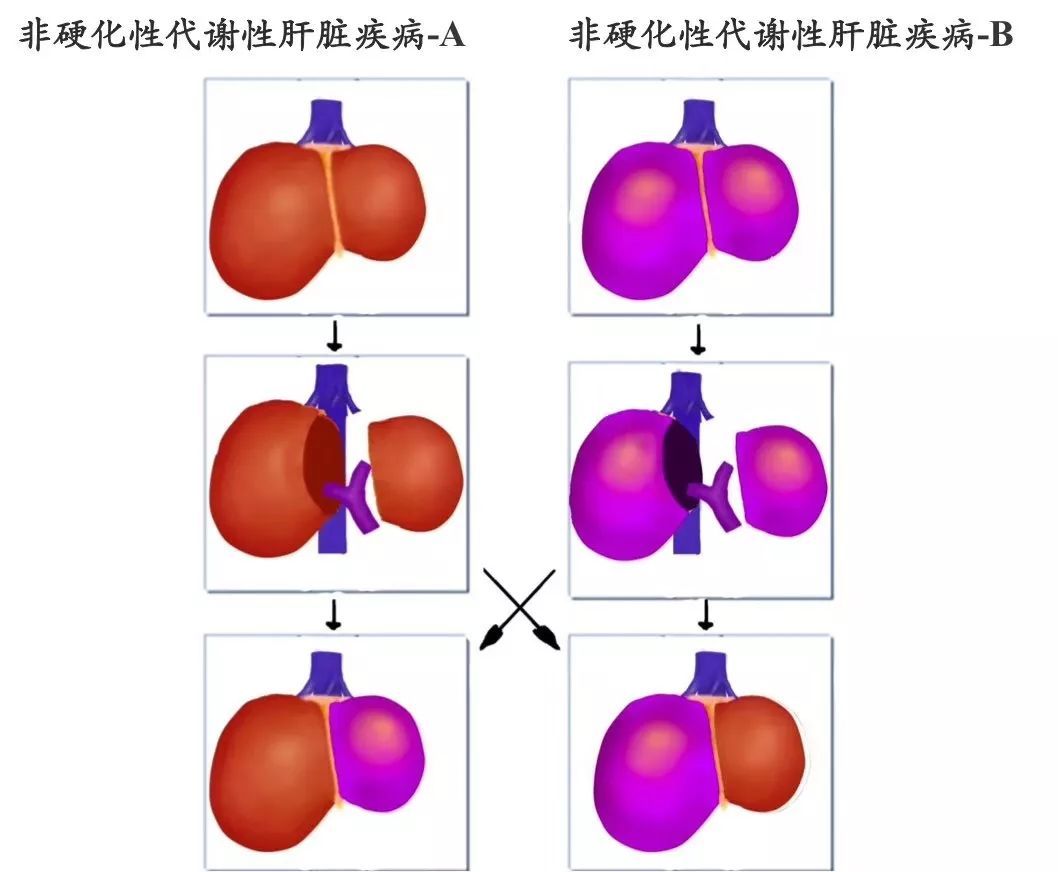
互换部分肝脏交叉辅助多米诺肝移植手术原理图示
从「首例」到「首例」
朱志军教授的想法虽然前所未有,但并非空中楼阁。
在肝脏移植领域,器官短缺是最关键、也最棘手的问题之一。面对这一世界范围的难题,多米诺肝脏移植(Domino Liver Transplantation,DLT)的概念应运而生。
朱志军教授作为通讯作者的《多米诺肝脏移植临床应用指南》中,对「多米诺肝脏移植」这样定义:
多米诺肝脏移植,是利用一名肝脏移植受者的病肝作为另一名患者的供肝移植物进行肝脏移植手术的治疗方式。
多米诺肝移植供者接受经典供肝来源方式(尸体供肝或活体供肝)的肝脏移植,治疗目的是根治或纠正自体肝脏疾病所导致的代谢缺陷。
作为多米诺供肝,除其存在特殊的代谢缺陷,肝脏其他的结构和功能是正常的,所以在特定的多米诺肝移植受者体内环境下,由于身体其他部位存在适当的代谢酶活性,多米诺供肝的代谢缺陷不会导致多米诺肝移植受者发生临床病理改变。
理想的多米诺供肝是其主要疾病不应导致多米诺肝脏移植受者出现新发获得性疾病,或仅出现临床上无意义的代谢变化。
《多米诺肝脏移植临床应用指南》
这一技术的出现不仅拯救了原本因器官短缺而等待的患者,同时也为像小航和小勇这样的遗传性代谢性肝病患者提供了治疗的机会。
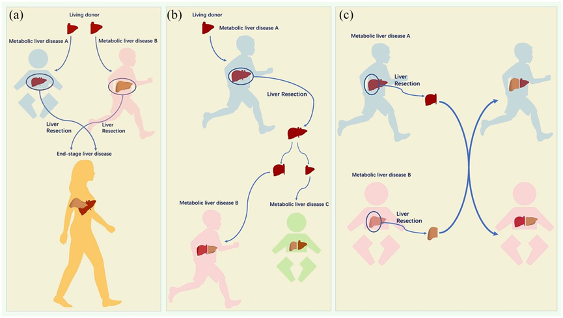
三种不同类型的多米诺肝脏移植:A 双多米诺供肝交叉辅助式肝脏移植;B 多米诺交叉辅助式肝脏移植;C 多米诺交叉互换式肝脏移植(图源:参考文献 6)
早在 2009 年,朱志军教授曾接诊过这样一对兄弟。弟弟要给哥哥捐肝进行移植,但评估后发现弟弟的肝脏比例不太合适,其左半肝只有 26%。
对于捐肝者而言,捐献后剩余的肝脏至少要占到 30~35% 才能保证供者的安全。如果弟弟捐右半肝,则残肝不够自身使用;如果捐左半肝又不够弟弟使用。
该怎么解决?巧合的是,病房里正有一名 8 岁的遗传代谢病女孩马上要进行肝移植手术。按照原本的计划,她的病肝在切除后即被废弃,但这个「废肝」除了草酸代谢异常以外,其他功能都正常。
那么,能不能用这个「废肝」和弟弟的左半肝合在一起?既解决肝脏过小的问题,健康的左半肝又可以辅助解决「废肝」的草酸代谢障碍。
幸运的是,经过家属知情同意和肝移植团队周密准备,这台手术取得了成功。目前,接受了两部分肝脏移植的哥哥已经健康生活了十余年。
首个案例的成功,成为了朱志军团队继续拓展创新的基石。
2013 年,朱志军团队完成了国内首次「双多米诺交叉辅助式肝移植」,将一名 Wilson 病患儿和一名 OTCD(鸟氨酸氨甲酰转移酶缺陷)患儿的肝脏组合起来,移植给了一位终末期肝脏疾病的患者。
2014 年,朱志军团队收治了 3 名代谢性疾病的患儿,分别为 13 岁 O 型血的高胆固醇血症患儿甲、12 岁 B 型血的 Wilson 病患儿乙、7 岁 AB 型血的尿素循环障碍患儿丙。
团队将一位脑死亡患者的健康肝脏整个移植给患儿甲,再将患儿甲的病肝一分为二,分别移植给患儿乙和丙,这两个患儿各保留原有的一半肝脏。
多年经验的积累,多个案例的成功,都在无形之中为「世界首例」打下了坚实的基础。

朱志军教授 2014 年发表论文节选
9 小时接力,完成「世界首例」
时间来到 2018 年 12 月 29 日,这是改变小航和小勇人生的一天——世界首例「两人互换部分肝脏交叉辅助多米诺肝移植手术」正式开始。
与传统的完整肝移植不同,部分肝移植意味着所有的吻合都需要在二级血管分支上做重建,血管更细更小,变异也更多。
「供体这一方的动脉可能是一支主干,而另一方则是多根分支,对于手术主刀来说,能够操作的空间非常小。」朱教授描述道。不仅如此,血管的吻合、胆道的重建也都需要提前预估,还要根据代谢情况来精准计算匹配,保证供体受体两侧的均衡。
为此,手术前朱志军教授团队运用数字影像技术构建了肝脏的三维透视图像,精确计算了移植肝脏的大小,以及两个肝脏上的每一条血管和胆管该如何利用,也在术前就精心设计、了然于胸。
朱志军团队分成两组,同时为小勇和小航进行手术。由于小勇的肝脏比小航的稍大一些,团队首先取小勇部分肝脏,并在体外进行修剪。趁着这个时间差,朱志军教授先为小勇做移植血管的吻合,再为小航进行同样操作。
「以往遗体来源的移植,可以完全从遗体中取足够多的血管,但在互换肝移植中没有多余的血管,因此需要尤其精准的操作。」朱志军教授介绍,为了以防术中发现吻合原位血管太短,团队提前取大网膜上血管作为备份。
朱志军团队在手术中
历经 9 小时,手术顺利结束。
术后,两名患者的血氨情况正常。小航的蛋氨酸在术后两周下降了 90%,接近正常水平;小勇的语言能力和肌张力也较术前也有了明显的改善。
进一步长期随访显示,术后数年里两位患儿仍然维持着健康的状态,没有代谢障碍的再发生。期间小航曾因青春期发育产生了轻微的排异反应,但也及时通过药物治疗稳定住了情况。
从人到器官,之后呢?
自开始从事肝移植工作以来,朱志军教授累计主刀完成了 3100 多例肝移植手术,其中儿童肝移植手术 1000 多例。「我们团队成员,除了我从 98 年开展肝移植工作,其他同事也都从零几年开始就接受肝脏移植训练。」
对于这样一个团队,创新并非偶然。「在开展交叉肝移植的时候,团队里工作年限最短的医生也已有 10 多年的经验积累了。」

由于代谢缺陷病通常较为罕见,朱志军教授还与北京友谊医院肝病中心主任贾继东教授联合创立了「代谢性肝病信息共享网络」,促进了交叉辅助式双多米诺供肝肝移植技术的推广和应用,让这项技术在全国各地的肝脏移植中心逐渐被认识。
「可以想象的东西很多,但不能拿人体去做实验。一定是病人有需求,又没有别的替代方法可以接受,才能付诸实践。」朱志军教授这样说。
在理念和实践的基础上,朱志军团队还提出了更多的创想。
「如果器官保存时间有限,能不能把其中的细胞提取出来。比如把代谢病患者肝脏细胞溶解下来长期体外保存,通过细胞移植来治疗婴幼儿急性肝衰,维持至患儿长大具备器官移植的手术条件。」类似这样的课题,朱志军团队还在不断探索与研究。
一把柳叶刀在朱志军教授的手中,成为了连接过去和未来的桥梁。挽救多个家庭的同时,也给患者提供了接受未来技术的可能性。
「在人类早期社会,群体通过抛弃患病个体的办法来维持种群稳定。后来医学技术出现,如今可以通过整个器官的移植来维持人的生存。而面向未来,我们走出了第一步。」朱志军教授这样解释他的器官移植理念。
「器官不是最小的单位,移植器官的一部分也可以维持人的生存。在更远的未来,随着医学技术的不断进步,还会有更精细的理解与划分。」
致谢:本文经 北京友谊医院肝脏移植中心主任 朱志军 专业审核
策划:z_popeye|监制:carollero




發表評論 取消回复